Группа - соль
Cтраница 1
Группа солей - самая многочисленная в ассортименте неорганических реактивов, и число их превышает 1000 наименований. С учетом химических свойств, местонахождения солеобразующих элементов в периодической системе элементов Д. И. Менделеева и по некоторым другим признакам неорганические соли подразделяют на девять подгрупп. [1]
Группа солей ( 1686) при термолизе в системе напуска также отщепляет НВг, но органическими продуктами разложения является тетратиофульвены. [2]
Эта группа солей крайне немногочисленна. [3]
В группах газообразных солей типа MmXOn ( M - катион -, а X - анионобразующий элемент, m 1 или 2), образующих изокатионные ряды, отчетливо прослеживается линейная зависимость АЛН солей от энтальпий атомизации газообразных анионобразующих оксидов, которую можно представить в виде уравнения: Аа Н ( МтХОп газ 298) кАа Н ( анионобразующий оксид. [4]
Наибольшее значение из этой группы солей имеют пентафтор-оксиниобат калия K2NbOF5 - H2O и гептафторотанталат калия K2TaF7, получившие промышленное применение. [5]
В результате омыления образуются две группы солей бария: растворимые в масле и не растворимые, которые выпадают в осадок и подлежат удалению. [6]
Один атом хлора хлорокиси и группа ONa соли кислоты обмениваются местами. [7]
Рассмотрение характера изменения энтальпий атомизации в группах солей, образующих изокатионные ряды, позволяет оценивать энтальпии атомизации и рассчитывать энтальпии образования не исследованных еще газообразных солей и корректировать полученные экспериментальные данные, выходящие за пределы линейной зависимости. Работоспособность предложенного критерия термической устойчивости газообразных солей и метода оценки их энтальпий атомизации и образования подтверждена экспериментально на десятках примеров. [8]
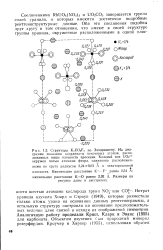 |
Структура KsUOaFs по Захариасену. На диаграмме показаны координаты некоторых атомов, расположенных выше плоскости проекции. Каждый ион UO22 окружен пятью атомами фтора, одинаково расположен. [9] |
Соединениями RbUO2 ( NO3b и UO2CO3 завершается группа солей уранила, о которых имеются достаточно подробные рентгеноструктурные данные. [10]
Уменьшение степени замещения ксантогената целлюлозы ( отщепление групп соли - OCSSNa) приводит к изменению физико-химических свойств вискозы: увеличению ее вязкости и понижению устойчивости к действию коагулянтов - электролитов. При рассмотрении этой кривой необходимо иметь в виду, что вискоза представляет собой концентрированный, по-видимому, коллоидный раствор ксантогената целлюлозы. Поэтому свойства вискозы отличаются от свойств истинных разбавленных растворов полимеров. [11]
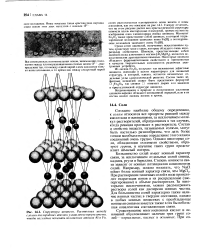 |
Структура шпинели. Расстояния между слоями кислородных атомов умышленно преувеличены, чтобы нагляднее показать положения атомов А1 и Fe. [12] |
Существование многоосновных кислот и оснований обусловливает наличие трех групп солей - нормальных, кислых и основных. [13]
Классическая теория кислот и оснований такие соли относит к группе негидролизующихся солей. С позиций же протолитической теории кислот и оснований нейтральный характер их растворов ( рН - 7) объясняется тем, что гидратированные ионы щелочных и некоторых щелочноземельных металлов, например Na ( H2O) n ], ICa2 ( H2O) n ] 2, вследствие крайне незначительного ион-дипольного взаимодействия представляют собой весьма слабые кислоты, а анионы сильных кислот, обладая в разбавленных растворах весьма малым сродством к протону, являются исключительно слабыми основаниями. [14]
Классическая теория кислот и оснований такие соли относит к группе негидролизующихся солей. С позиций же протолитической теории кислот и оснований нейтральный характер их растворов ( рН 7) объясняется тем, что гидратированные ионы щелочных и некоторых щелочно-земельных металлов, например [ Ыа ( Н2О) ], [ Са2 ( НгО) п ] 2, вследствие крайне незначительного ион-диполь-ного взаимодействия представляют собой весьма слабые кислоты, а анионы сильных кислот, обладая в разбавленных растворах весьма малым сродством к протону, являются исключительно слабыми основаниями. [15]
Страницы: 1 2 3 4