Оксидная группа
Cтраница 1
 |
Результаты расчетов по методу CNDO значений энергии. [1] |
Оксидная группа в феноксид-ионе является очень сильно активирующим заместителем, сильнее даже, чем NR2, и более орто-ориентирующим, чем гидроксильная группа. Результаты расчетов, приведенные в табл. 3.2, свидетельствуют, что в феноксид-ионе электронная плотность в орго-положении выше, чем в ара-положении; в нейтральных молекулах эта разница не столь заметна. [2]
Оксидная группа оказывает двойственное электронное влияние. С одной стороны, она действует как сильный резонансный донор электронов за счет отрицательно заряженного атома О, а с другой - как сильный индуктивный акцептор электронов за счет положительно заряженного атома N. Именно благодаря донорному эффекту N-оксидной группы значительно увеличивается электронная плотность на Сз по сравнению с С4, и на нем наводится отрицательный заряд. [3]
Оксидная группа оказывает двойственное электронное влияние. С одной стороны, она действует как сильный резонансный донор электронов за счет отрицательно заряженного атома О, а с другой - как сильный индуктивный акцептор электронов за счет положительно заряженного атома N, Именно благодаря донорному эффекту N-оксидной группы значительно увеличивается электронная плотность на С3 по сравнению с Сд, и на нем наводится отрицательный заряд. [4]
Большинство методов количественного определения оксидной группы основано на легкости присоединения этиленоксидами хлористого или бромистого водорода и образования этиленхлор - или этиленбром-гидринов. Последние определяют алкалиметрическим или ацидиметриче-ским титрованием. [5]
Широкое применение имеет определение оксидных групп, основанное на взаимодействии вещества с галогеноводородными кислотами в неводных растворителях. [6]
Большинство методов количественного определения оксидной группы основано на легкости присоединения этиленоксидами хлористого или бромистого водорода и образования этиленхлор - или этиленбром-гидринов. Последние определяют алкалиметрическим или ацидиметриче-ским титрованием. [7]
Широкое применение имеет определение оксидных групп, основанное на взаимодействии вещества с галогеноводородными кислотами в неводных растворителях. [8]
Если а-положение к Л - оксидной группе занято алкильным радикалом, то замещение происходит именно в нем. Аналогичные реакции замещения наблюдаются и с фосфорилгалогенидами. [9]
На ДИП раствора II наблюдаются пики восстановления оксидной группы при N 4 и обеих азомети-новых групп. [10]
Благодаря тому, что кислород Д - оксидной группы является электронодонорным заместителем, а азот гетерокольца несет положительный заряд и, следовательно, является акцептором электронов, эти соединения обладают ценным комплексом свойств, широко используемым в синтезе. [11]
На ДИП раствора IV идентифицированы 4 пика восстановления оксидной группы при N 4, 4 5-азометиновой группы, карбонильной группы и 1 2-азометиновой группы с Еи - 0 480, - 0 680, - 0 980 и-1 190В ( нас. [12]
 |
Относительные скорости рс-ами, Х - оксидов хлорпиридазинов с пиперидином ( при 50 С. [13] |
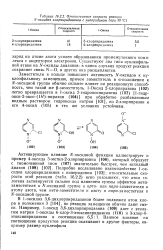
Заместители в кольце повышают активность yV - оксидов к ну-клеофильному замещению, причем заместитель в а-положении к jV - оксидной группе обычно сильнее влияет на реакционную способность, чем такой же ( - заместитель. Оксид 2-хлорпиразипа ( 102) легко превращается в 1-оксид 2-гидроксипиразнна ( 103) [ 1-гидр-окси - 2-оксо - ( 1 Я) - пиразин ( 104) ] при обработке разбавленным водным раствором гидроксида натрия [101], но 2-хлорпиразин и его 4-окснд ( 105) в тех же условиях устойчивы. [14]
 |
Относительные скорости реакции N-оксидов хлорпиридазинов с пиперидином ( при 50 С. [15] |
Страницы: 1 2 3