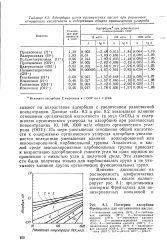
Неионизированная карбоксильная группа
Cтраница 1
Неионизированная карбоксильная группа Glu-35 выступает в качестве донора протона, поставляя его гликозидному атому кислорода между атомом Qi сахара D и Ci4, сахара Е ( стадия общего кислотного катализа); это приводит к разрыву гликозидной связи. В результате остаток сахара D переходит в состояние карбкатиона с положительно заряженным атомом углерода Qn и принимает конформацию полукресла. Отрицательный заряд карбоксилатной группы Asp-52 стабилизирует карбкатион. Остаток NAGa ( сахара Е - f - F) диффундирует из области активного центра. Остаток NAG4 ( сахара D C B А) уходит из области активного центра, и фермент возвращается в исходное состояние. [1]
По мнению авторов, лимитирующей стадией превращения в этом случае является взаимодействие неионизированной карбоксильной группы с соседней нитроани-лидной группой. [2]
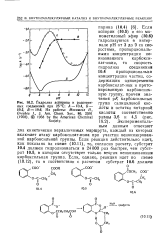 |
Гидролиз аспирина и родствен-ных соединений при 25 С. Л -, Б -, Я-10. 6. Из работы. Morawetz Н., Oreskes L, J. Am. Chem. Soc., 80, 2591 ( 1958. 1958 by the American Chemical Society. [3] |
Два кинетически неразличимых маршрута, каждый из которых включает атаку карбоксилат-иона при участии неионизированной карбоксильной группы. Если реакция действительно идет, как показано на схеме (10.11), то, согласно расчету, субстрат 10.4 должен гидролизоваться в 24000 раз быстрее, чем субстрат 10.5, в котором отсутствует только вторая неионизованная карбоксильная группа. [4]
При сравнении ИК спектров колхицидил - L - лизина и диколхи-цидильного производного в области карбонила неионизированной карбоксильной группы обнаруживается появление соответствующего поглощения при 1729 см в дизамещенном производном 8 и отсутствие такового в монопроизводном 5 Это обстоятельство представляет собой дополнительное веское доказательство а / - замещения в колхицидил - L - лизине и, следовательно, колхицидил - L - орнитине тоже. [5]
По мере уменьшения отношения общей кислотности к содержанию органического углерода адсорбция увеличивается вследствие уменьшения влияния ионизированной или неионизированной карбоксильной группы. Аналогично, в кислой среде неионизированные карбоксильные группы приводят к возрастанию адсорбционной емкости угля на один порядок по сравнению с емкостью угля в щелочной среде. Эти зависимости были получены только для карбоксильных групп и не учитывают влияния других органических функциональных групп. [7]
Во втором типе комплексов кроме полос 1645 - 1635 и 1480 - 1460 имеется полоса поглощения при 1710 - 1705 см -, относящаяся к неионизированной карбоксильной группе СООН, которая образует водородную связь с соседними молекулами. Комплексы этого типа обнаружены для гафния с ИМДА и гафния и циркония с ДЭТПА. [8]
По мере уменьшения отношения общей кислотности к содержанию органического углерода адсорбция увеличивается вследствие уменьшения влияния ионизированной или неионизированной карбоксильной группы. Аналогично, в кислой среде неионизированные карбоксильные группы приводят к возрастанию адсорбционной емкости угля на один порядок по сравнению с емкостью угля в щелочной среде. Эти зависимости были получены только для карбоксильных групп и не учитывают влияния других органических функциональных групп. [9]
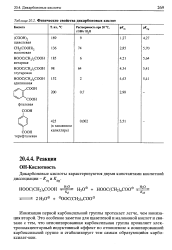 |
Физические свойства дикарбоновых кислот. [10] |
Ионизация первой карбоксильной группы протекает легче, чем ионизация второй. Это особенно заметно для щавелевой и малоновой кислот и связано с тем, что неионизированная карбоксильная группа проявляет элек-троноакцепторный индуктивный эффект по отношению к ионизированной карбоксильной группе и стабилизирует тем самым образующийся карбо-ксилат-ион. [11]
Существенно, что именно ферментативно связанная оксалилуксусная кислота ( НООС-СО-СН2-СОО-фер-мент) осуществляет окисление ацетата, обеспечивая связывание с реакционноспособной карбонильной группой, с которой может соединяться эфир ацетил-кофермент А. В такой связанной оксалилуксусной кислоте углеродный центр карбонильной группы является очень электрофильным вследствие индуктивного оттягивания электронов от этого центра как свободной неионизированной карбоксильной группой, так и связанной кар-боксилатной группой. [12]
Протонированные аминогруппы ( имидазолий, аммоний и гуанидиний) взаимодействуют с отрицательно заряженными группами, например карбокси-латной, оксианионами и галогенид-ионами, и с нейтральными акцепторными группами, например кислородными атомами воды или карбонильным кислородом ионизированных карбоксильных групп, но не с карбонильным кислородом амидных групп. Нейтральная группа N - Н амидной группы взаимодействует преимущественно с карбонильным кислородом ацильных, амидных или ионизированных карбоксильных групп; взаимодействия с карбокси-латными группами и галогенид-ионами наблюдаются лишь в редких случаях. Малочисленность данных, относящихся к незаряженным имддазольнрйиин - jJ9ДьЖЩJCДШШl t H, не позволяет делать какие-либо Обобщения относительно их взаимодействийтТидроксильная группа независимо от того, является ли она боковой группой, принадлежит ли неионизированной карбоксильной группе или молекуле воды, обнаруживает тенденцию к взаимодействию с карбоксилатными группами, кислородом и анионами галогенов, карбонильными атомами кислорода и атомом кислорода в молекулах воды. [13]
Поэтому они могут участвовать в ионных взаимодействиях. Эти остатки определяют отрицательный вклад в общий заряд белковой молекулы. Они могут также участвовать в образовании водородных связей. Неионизированная карбоксильная группа служит хорошим донором водорода, а карбоксилат-ион - хорошим актептором. Амиды, образуемые этими карбоксилатными группами ( остатки глутаминовой и аспарагиновой кислот), могут участвовать в образовании водородных связей точно так же, как и амидные группы полипептидной цепи. Карбоксилатные группы могут также принимать участие в образовании клешневидных комплексов с ионами металлов, которые нередко прочно связаны с белками. [14]
В пользу того, что аминокислоты имеют биполярную структуру, говорит и ряд других данных. Так, например, как уже было указано в разд. III, нейтральные растворы аминокислот имеют высокий положительный инкремент диэлектрической проницаемости, что и должно наблюдаться для биполярных ионов. Растворение аминокислот в воде сопровождается значительным уменьшением объема, что объясняется уплотнением воды при взаимодействии с заряженными группами биполярного иона кислоты. Как и большинство ионных кристаллов, аминокислоты лучше растворяются в воде, нежели в неполярных растворителях. В спектрах комбинационного рассеяния твердых или растворенных аминокислот, находящихся в катионной форме и только в этом случае), наблюдается сильная линия при 1740 см-1, соответствующая частоте характеристических валентных колебаний неионизированной карбоксильной группы. Вместе с тем две линии в области около 3350 слг1, характерные для незаряженной аминогруппы, наблюдаются только для анионной формы аминокислот. В пользу биполярной структуры аминокислот свидетельствуют также и другие спектральные данные. [15]
Страницы: 1