L-слой
Cтраница 1
L-слой содержит всего четыре орбпталп одну s - и три р-орбпталн) и не может вместить более восьми электронов. [1]
L-слоя в следующий ( не обозначенный на таблице) М - слой, но на это нужно было бы затратить слишком большую энергию, которую не смогла бы компенсировать энергия, освобождающаяся при образовании соответствующей связи. [2]
L-слоя этого элемента, то в случае ординарных связей атома фосфора вопрос представляется более сложным. [4]
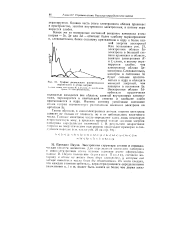 |
График радиального распределения вероятности в атоме натрия. [5] |
К-и L-слоев; 2 - для Зз-элек-трона; 3 - для Зр-электрона. [6]
Формирование L-слоя ( я 2) начинается с лития, у которого имеется три электрона. Два первых электрона, как у гелия, заполняют / ( - слой. Третий электрон лития не может находиться в этом слое, так как на 1 s - орбитали электронных вакансий нет. Помещение третьего электрона на s - орбиталь, максимальная электронная емкость которой равна двум, противоречило бы принципу Паули. У последнего элемента второго периода неона все s - и р-орбитали при п 2 заполнены. В ней квадратные скобки символизируют электронные структуры благородных газов, которые органически входят в строение атомов последующих элементов. [7]
Таким образом, L-слой неона оказывается полностью застроенным и на этом элементе завершается второй период периодической системы Менделеева. [8]
Таким образом, L-слой неона оказывается полностью застроенным, и на этом элементе завершается второй период периодической системы Менделеева. [9]
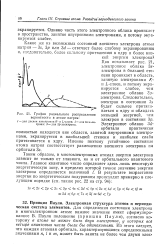 |
График радиального распределения. [10] |
К - и L-слоев; 2 - для 35 - э ек-трона; 3 - для Зр-электроиа. [11]
 |
График радиального распределения вероятности в атоме натрия. [12] |
К - и L-слоев; 2 i для Ss-электрона; 3 - для Зр-электрона. [13]
Начиная с лития формируется L-слой ( л 2), так как попадание третьего электрона в первый слой означало бы ( Нарушение запрета Паули. Второй слой завершается у неона; у него заполнены и s - и р-оболочки. От натрия до аргона комплектуется третий слой, подобно второму. [14]
Начиная с лития формируется L-слой ( п 2), так как попадание третьего электрона в первый слой означало бы нарушение запрета Паули. Второй слой завершается у неона; у него заполнены и s - и р-обблочки. От натрия до аргона комплектуется третий слой подобно второму. [15]
Страницы: 1 2 3 4
