Гидроксильная группа - силикагель
Cтраница 1
Гидроксильные группы кальциевого силикагеля в отличие от силаноль-ных групп силикагеля должны иметь основной характер. [1]
Все гидроксильные группы силикагеля могут реагировать, по 153 ], с Са ( ОН) 2, если концентрация последнего достаточно высока и поверхность Si02 доступна для ионов. Если принять такую схему взаимодействия компонентов при известковой активации ( сопровождаемую удалением двух молекул воды за счет двух гидрок-сйлов SiOH), то количество ОН-групп на поверхности адсорбента в результате должно резко уменьшиться. [2]
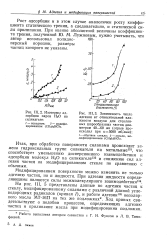 |
Изотермы ад.| Зависимость числа адгезии от относительной влажности воздуха для стеклянных шарообразных частиц диаметром 40 - 60 мк ( отрыв происходил при 5000 об / мин.. [3] |
Итак, при обработке поверхности силанами происходит замена гидроксильных групп силикагеля на метальные131, что способствует уменьшению дисперсионного взаимодействия и адсорбции молекул Н2О на силикагеле132 и снижению сил адгезии частиц на модифицированном стекле по сравнению с обычным. [4]
Методом ИК-спектроскопии было показано, что в результате замещения гидроксильных групп силикагеля на атомы фтора свободных гидроксильных групп на поверхности практически не остается [16], а оставшиеся гидроксильные группы возмущены в результате образования водородной связи OH... В связи с этим адсорбция воды и метанола на частично фторированной поверхности силикагеля невелика. В случае метилированных образцов образование водородной связи между ОН - и СН3 - группами исключено, и оставшиеся доступными гидроксильные группы являются свободными и принимают участие в адсорбции полярных веществ. [5]
Методом ИК-спектроскошш было показано, что в результате замещения гидроксильных групп силикагеля на атомы фтора свободных гидроксильных групп на поверхности практически не остается [16], а оставшиеся гидроксильные группы возмущены в результате образования водородной связи OH... В связи с этим адсорбция воды и метанола на частично фторированной поверхности силикагеля невелика. В случае метилированных образцов образование водородной связи между ОН - и СН3 - группами исключено, и оставшиеся доступными гидроксильные группы являются свободными и принимают участие в адсорбции полярных веществ. [6]
В [369] показано, что при одной и той же степени замещения гидроксильных групп силикагеля фтором или органическими группами ( метальными, этильными, пропиль-ными и другими насыщенными радикалами) падение величин адсорбции полярных веществ не одинаково. [7]
На этом основании был сделан вывод об отсутствии различия в подвижности протонов гидроксильных групп силикагеля и алюмосиликагеля. [8]
Метод количественной оценки дополнительного вклада ( связанного с взаимодействием л-электронов бензола с диполями гидроксильных групп силикагеля) в энергию адсорбции молекулы бензола гидратированной поверхностью силикателя представляется мне необоснованным. Этот метод, развитый А. В. Киселевым в многочисленных публикациях, не учитывает изменения в текстуре поверхности силикагеля при его дегидратации. Несколько упрощая вопрос, можно сказать, что если гидратированная поверхность силикагеля представляет собой плотный частокол гидроксильных групп, то предельно дегидратированная поверхность может быть охарактеризована как вдвое более разреженный частокол кислородных ионов. Поэтому понижение энергии адсорбции, например бензола, при дегидратации будет вызвано не только исчезновением специфического ( по терминологии А. В. Киселева) взаимодействия, но и уменьшением дисперсионной компоненты взаимодействия. Вот почему мне кажутся неубедительными расчеты, приведенные в статье А. В. Киселева и В. И. Лыгина ( стр. [9]
Практическое применение предлагаемого метода иллюстрируется нами на примере радиационного изотопного обмена дейтерия с гидроксильными группами силикагеля. Выбор конкретного объекта исследования обусловлен личными научными интересами авторов. Принципиальное значение работы от выбора конкретного объекта не зависит. [10]
Тип П - специфические адсорбенты, имеющие на поверхности локально сконцентрированные положительные заряды, например гидроксильные группы силикагелей, катионы цеолитов. [11]
Тип II - специфические адсорбенты, имеющие на поверхности локально сконцентрированные положительные заряды, например гидроксильные группы силикагелей, катионы цеолитов. [12]
Метод количественной оценки дополнительного вклада ( связанного с взаимодействием it - электронов бензола с диполями гидроксильных групп силикагеля) в энергию адсорбции молекулы бензола гидратированной поверхностью силикателя представляется мне необоснованным. Этот метод, развитый А. В. Киселевым в многочисленных публикациях, не учитывает изменения в текстуре поверхности силикагеля при его дегидратации. Несколько упрощая вопрос, можно сказать, что если гидратированная поверхность силикагеля представляет собой плотный частокол гидроксршь-ных групп, то предельно дегидратированная поверхность может быть охарактеризована как вдвое более разреженный частокол кислородных ионов. Поэтому понижение энергии адсорбции, например бензола, при дегидратации будет вызвано не только исчезновением специфического ( по терминологии А. В. Киселева) взаимодействия, но и уменьшением дисперсионной компоненты взаимодействия. Вот почему мне кажутся неубедительными расчеты, приведенные в статье А. В. Киселева и В. И. Лыгина ( стр. [13]
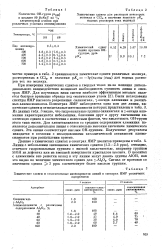 |
Количество ОН-групп в цеолите 90 DcNaY на. [14] |
При измерении химических сдвигов в твердых телах из-за влияния диполь-дипольного взаимодействия возникает необходимость суживать линии в спектрах ЯМР. Были исследованы спектры ЯМР высокого разрешения силикагеля, 7 оксида алюминия и различных алюмосиликатов. Из данных табл. 3 видно, что гидроксильные группы силикагеля и у-оксида алюминия характеризуются небольшими, близкими друг к другу значениями химического сдвига в соответствии с известным фактом, что кислотность ОН-групп этого типа низка. Для алюмосиликатов со средним содержанием алюминия появляется дополнительная линия с относительно высоким значением химического сдвига. Эта линия соответствует кислым ОН-группам. Полученные результаты находятся в согласии с исследованиями каталитической активности алюмосиликатов при расщеплении кумена. [15]
Страницы: 1 2