Енольная гидроксильная группа
Cтраница 1
Енольная гидроксильная группа может участвовать в образовании хелатного цикла. [1]
Так, енольная гидроксильная группа его может присоединяться к этилиденовой двойной связи. По этой реакции в растениях родов Rauwolfia и Cotynanthe образуется молекула алкалоида аймалицина 6.480 - представителя группы природных оснований, называемых гетероиохимбановыми. [2]
Следует иметь в виду, что диазометан реагирует также с ароматическими и енольными гидроксильными группами. [3]
Отсутствие полосы поглощения при частотах более 3450 см 1 указывает на отсутствие енольной гидроксильной группы. [4]
Установлено, что вещество, вызывающее геморрагическое заболевание крупного рогатого скота и содержащееся в клевере, является 3 3 -метилен-б с - ( 4-оксикумарином) ( L, R Н) [174-177], который образует диметиловый эфир по двум кислым енольным гидроксильным группам. [5]
Но моногидразон ( II) не дает реакции на енольную гидроксильную группу - не растворяется в щелочи и не реагирует с эфирным раствором диазометана, что опровергает такое допущение. [6]
Стипитатовая и стипитатоновая кислоты. Стипитатовая кислота содержит одну карбоксильную группу и две фенольные или енольные гидроксильные группы. [7]
При кипячении аскорбиновой кислоты с избытком щелочи расход щелочи больше, что обусловлено частичным расщеплением лактонного кольца. На холоду или в теплом водно-спиртовом растворе удается точно определить одну из двух енольных гидроксильных групп. Следовательно, при работе с природными веществами неизвестного состава необходимо определять количество щелочи, потребляемой на холоду, при нагревании и после кипячения вещества с избытком щелочи. [8]
При кипячении аскорбиновой кислоты с избытком щелочи расход щелочи больше, что обусловлено частичным расщеплением лактонного кольца. На холоду или в теплом водно-спиртовом растворе удается точно определить одну из двух енольных гидроксильных групп. Аминокислоты 49 титруют спиртовой щелочью ( стр. Следовательно, при работе с природными веществами неизвестного состава необходимо определять количество щелочи, потребляемой на холоду, при нагревании и после кипячения вещества с избытком щелочи. [9]
Трополоны обладают фенольными свойствами ( положительная реакция с хлорным железом) и по своей кислотности ( р / С-7) занимают промежуточное положение между фенолом и уксусной кислотой. Они вступают в реакции замещения с бромом и азотной кислотой и сочетаются с диазотированными аминами. Их енольная гидроксильная группа легко алкилируется ( диазометаном), но ацилируется с некоторым трудом. Трополоны устойчивы к окислению перманганатом калия и нелегко гидрируются; они не проявляют явных кетонных свойств, хотя после полного или частичного гидрирования кетогруппа реагирует нормально. [10]
Трополоны обладают фенольным и свойствами ( положительная реакция с хлорным железом) и по своей кислотности ( рК - 7) занимают промежуточное положение между фенолом и уксусной кислотой. Они вступают в реакции замещения с бромом и азотной кислотой и сочетаются с диазотиро вавными аминами. Их енольная гидроксильная группа легко алкилируется ( диазометаном), но ацилируется с некоторым трудом. Трополоны устойчивы к окислению перманганатом алия и нелегко гидрируются; они не проявляют явных кетонных свойств, хотя после - полного или частичного гидрирования кетогруппа реагирует нормально. [11]
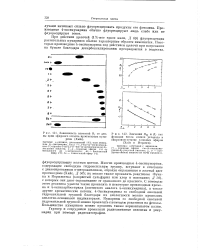 |
Значения RM и R / как. [12] |
Многие производные 4-оксикумарина, содержащие свободную гидроксильную группу, вступают в сочетание с диазотированным / г-нитроанилином, образуя окрашенные в желтый цвет производные ( Хайс, Д 50); их можно также проявлять реактивом Фучика и Коржистека ( хлористый сульфурил или хлор и основание; Д 70), с которым они дают окрашивание от оранжевого до красного. С помощью этого реактива удается также проявлять и некоторые производные хромо-на и 4-оксикарбостирила ( азотистого аналога 4-оксикумарина), а также другие ароматические кетоны. Оксикумарины со свободной енольной гидроксильной группой благодаря их кислотности можно проявлять, кислотно-основными индикаторами. Кумарины со свободной енольной гидроксильной группой можно проявлять с помощью реактивов на фенолы. [13]
Положение этого равновесия зависит от различных факторов, например от природы растворителя. По химическим свойствам енолы отчасти сходны с фенолами. Так, енольная гидроксильная группа гораздо кислее, чем спиртовая, и в этом отношении близка к фенольному гидроксилу. Химические свойства енолов определяются присутствием гидро-ксила ( они могут ацилироваться или давать простые эфиры) и двойной связи. Так как между енолами и рассматриваемыми ендио-лами, или редуктонами, нет резкого различия, некоторые реакции являются для них общими. [14]
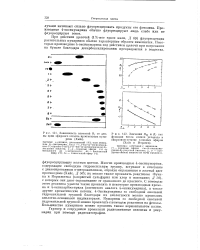 |
Значения RM и R / как. [15] |
Страницы: 1 2