Иминоксильная группа
Cтраница 1
Иминоксильная группа обычно сохраняется, но низкие выходы основного продукта показывают, что реакция часто осложняется побочными процессами. Особенность взаимодействия этого кетон-радикала с нуклеофильными реагентами заключается в том, что последние, обладая неподеленными электронными парами, могут использовать их не только для образования новой связи с углеродным атомом карбонильной группы, но и для восстановления иминоксильной группы. В определенных условиях реакция восстановления может оказаться преобладающей ( гидразин, алкилмагнийгалогенид), поэтому при подборе нуклеофиль-ных реагентов приходится учитывать их восстановительные свойства. [1]
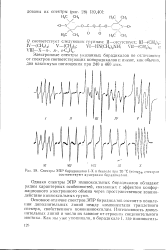 |
Спектры ЭПР бирадикалов 1 - Х в бензоле при 20 С соответствуют нумерации бирадикалов. [2] |
Однако спектры ЭПР иминоксильных бирадикалов обладают рядом характерных особенностей, связанных с эффектом конфор-мационного электронного обмена через пространственное взаимодействие иминоксильных групп. [3]
Равновесие обычно полностью сдвинуто в сторону енамина ИМИНОКСИЛЬНЫЕ РАДИКАЛЫ ( нитроксилы, нитро-ксиды), нейтральные частицы с неспаренным электроном на иминоксильной группе N-О. Образуются при окислении иминов, гидро-ксиламинов, из нитронов, нитрозо - и нитросоединений. [4]
Этерификация гидроксильной группы осуществляется гораздо труднее, чем гидролиз сложноэфирной группы, так как применяемые при этерификации кислотные катализаторы взаимодействуют с иминоксильной группой, а в отсутствие кислот реакция протекает очень медленно. Практически единственным методом препаративного получения сложных эфиров из карбоновых кислот, содержащих иминоксильную группу, является взаимодействие кислот с диазосоединениями. [5]
Наличие такой суперсверхтонкой структуры в спектрах ЭПР других исследованных радикалов [11 -13], по-видимому, указывает на отличную от нуля вероятность нахождения неспаренного электрона за пределами иминоксильной группы радикала. [6]
Наличие гидроксильной группы в этом радикале мало сказывается на его стабильности, так как окислительный потенциал окси-группы здесь достаточно высок, чтобы при обычных температурах возможно было восстановление иминоксильной группы за счет гидроксильной. Индуктивное влияние обеих групп друг на друга также незначительно, поэтому они могут вступать в реакции практически независимо друг от друга. [7]
Измерение дипольного момента 2 2 6 6-тетраметил - 1-оксипипе-ридина позволяет определить величину момента группы С-NO - С диамагнитной молекулы. Следовательно, наличие неспаренного электрона увеличивает дипольный момент иминоксильной группы на 1 7D по сравнению с дипольным моментом группы в соответствующей молекуле. [8]
Этерификация гидроксильной группы осуществляется гораздо труднее, чем гидролиз сложноэфирной группы, так как применяемые при этерификации кислотные катализаторы взаимодействуют с иминоксильной группой, а в отсутствие кислот реакция протекает очень медленно. Практически единственным методом препаративного получения сложных эфиров из карбоновых кислот, содержащих иминоксильную группу, является взаимодействие кислот с диазосоединениями. [9]
Иминоксильная группа обычно сохраняется, но низкие выходы основного продукта показывают, что реакция часто осложняется побочными процессами. Особенность взаимодействия этого кетон-радикала с нуклеофильными реагентами заключается в том, что последние, обладая неподеленными электронными парами, могут использовать их не только для образования новой связи с углеродным атомом карбонильной группы, но и для восстановления иминоксильной группы. В определенных условиях реакция восстановления может оказаться преобладающей ( гидразин, алкилмагнийгалогенид), поэтому при подборе нуклеофиль-ных реагентов приходится учитывать их восстановительные свойства. [10]
Во-первых, имеется сильная стереоспецифичность констант СТВ с протонами. В сыи-формах ан больше, чем в анты-формах; в радикалах XXXI-XXXIII наблюдается СТВ лишь с протонами в Чыс-конформациях. В радикале XXXIV наблюдается СТВ с р-про-тонами и экваториальным у-протоном, который отделен пятью связями от атома кислорода иминоксильной группы, но не наблюдается СТВ с аксиальным протоном. Значения-констант а, и а близки. [11]
Равновесие обычно полностью сдвинуто в сторону енамина ИМИНОКСИЛЬНЫЕ РАДИКАЛЫ ( нитроксилы, нитро-ксиды), нейтральные частицы с неспаренным электроном на иминоксильной группе N-О. Образуются при окислении иминов, гидро-ксиламинов, из нитронов, нитрозо - и нитросоединений. Вступают в радикальные р-ции, а также в р-ции без участия иминоксильной группы. [12]
Страницы: 1