Небелковая простетическая группа
Cтраница 1
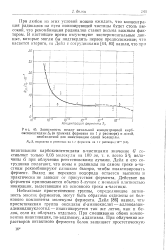 |
Зависимость между начальной концентрацией оксипептидазы SQ ( в граммах фермента на 1 г раствора и необходимой для инактивации одной молекулы. [1] |
Небелковые простетические группы, определяющие активность многих ферментов, могут быть обратимо отделены от белкового компонента молекулы фермента. Дейл [86] нашел, что простетическая группа оксидазы rf - аминокислот-аллоксазин-адениндинуклеотид - инактивируется так же легко, как и белок, если их облучать отдельно. При смешивании обоих компонентов инактивация, ло-видимому, аддитивна. [2]
Сложные белки, состоящие из белкового компонента и небелковой простетической группы, распадаясь в организме человека и животных, дают мочевину и ряд других конечных продуктов. [3]
Многим ферментам, катализирующим широкий спектр биохимических реакций, необходимо для эффективного осуществления каталитической функции присутствие небольшой небелковой простетической группы, более или менее прочно связанной с белком. Если эта небелковая группа обслуживает два ( или более) фермента, благодаря чему между ними может происходить перенос групп, то ее обычно называют коферментом. В ферментативной реакции различия между субстратом и коферментом не всегда ясны, так как кофермент, подобно субстрату, может в ходе реакции претерпевать структурные изменения. Однако при последующих реакциях первоначальная структура кофермента обычно восстанавливается, тогда как субстрат подвергается дальнейшим химическим превращениям. В тех случаях, когда кофермент на определенной стадии реакции оказывается структурно измененным, различие между коферментом и субстратом выявляется именно на основании этой конечной регенерации структуры. [4]
Ферменты представляют собой вещества или чисто белковой структуры, или протеиды - белки, связанные с небелковой простетической группой. Число уже известных ферментов очень велико. Считают, что одна клетка бактерии использует до 1000 разных ферментов. Однако лишь для немногих установлено строение. Примерами чисто белковых ферментов могут служить протеолитические ферменты пищеварения, такие, как пепсин и трипсин. Известны случаи, когда один и тот же белок несет в организме и структурную и ферментативную функцию. [5]
В процессе ферментативного катализа субстрат, временно образующий комплекс с ферментом, или, в некоторых случаях, небелковая простетическая группа играют роль примесей, собственные электронные уровни которых лежат вблизи зоны проводимости или валентной зоны белковой структуры. Таким образом, комплекс субстрат-фермент может рассматриваться как примесный полупроводник с электронной или дырочной проводимостью. Электрон, попавший в зону проводимости, не может спуститься в полностью занятую валентную зону и будет мигрировать вдоль цепочек водородно-пептидных связей до тех пор, пока не попадет в потенциальную яму акцептора, образовавшего комплекс с ферментом. [6]
Среди белков, наделенных ферментативными свойствами, можно обнаружить не только простые белки, не имеющие обособленных простетических групп ( к числу которых принадлежат, например, различные гидролазы), но и типичные сложные белки ( протеиды), состоящие из белкового компонента и небелковой простетической группы. К числу таких ферментов - протеидов - относится, в частности, ряд ферментов, катализирующих различные окислительно-восстановительные процессы. [7]
Среди белков, наделенных ферментативными свойствами, можно обнаружить не только простые белки, не имеющие обособленных простетических групп ( к числу которых принадлежат, например, различные гидролазы), но и типичные сложные белки ( протеиды), состоящие из белкового компонента и небелковой простетической группы. К числу таких ферментов - протеидов - относится, в частности, ряд ферментов, катализирующих различные окислительно-восстановительные процессы. [8]
 |
Примеры коферментов. [9] |
В то время как большинство ферментов состоит, по-видимому, исключительно из аминокислотных остатков, некоторые ферменты содержат и иные, не аминокислотные группы, каталитически активные в реакциях переноса. Такие ферменты можно рассматривать как состоящие из двух частей - белкового апофермента и небелковой простетической группы. [10]
В живых организмах многообразные химические превращения протекают на поверхностях высокоспециализированных катализаторов - ферментов. Все исследованные до настоящего времени ферменты в химическом отношении представляют собой либо чистые белки, либо сложные белки с небелковыми простетическими группами. Таким образом, биокатализ является по существу гетерогенным катализом на поверхностях белковых макромолекул. Рассмотрим, например, схему процессов тканевого дыхания, образующих так называемый главный путь окисления веществ в клетках и являющихся основным источником энергии, необходимой для жизнедеятельности. Суммарная реакция в конечном итоге приводит к переносу водорода окисляемого субстрата к кислороду воздуха и образованию воды; однако она разбивается на множество отдельных ступеней, сопровождающихся постепенным понижением потенциала системы. [11]
Уреаза катализирует гидролиз мочевины до двуокиси углерода и аммиака. В настоящее время в чистом или почти чистом виде известны сотни ферментов. Все они - белки, некоторые содержат также небелковые простетические группы, необходимые для действия ферментов. [12]
Страницы: 1