Поверхностная группа
Cтраница 3
Большинство рассмотренных данных о сдвиге полос поверхностных групп ОН относится к системам, в которых имеет место физическая адсорбция. [31]
Обычно невозможно удалить с поверхности гетероатомы или поверхностные группы; происходит образование других стабильных соединений, иногда содержащих поверхностные атомы объемной структуры. [32]
В результате таких воздействий могут изменяться не только концевые поверхностные группы, но и функциональные группы, лежащие в глубине полимерного тела. [33]
Отличительной чертой хемосорбции является необратимость изменений спектра поверхностных групп и хемосорбированных молекул. Общая картина взаимодействия усложняется также тем, что очень часто, например при адсорбции спиртов и аммиака, молекулярная адсорбция сопровождается частичной хемо-сорбцией. [34]
Асбест может вступать в реакцию за счет поверхностных групп. Этим объясняется большая сорбционная способность асбеста по отношению к гидроксидам металлов. По отношению к щелочам асбест является одним из самых устойчивых минералов, но он легко реагирует с кислотами, в процессе чего из минерала активно извлекаются оксиды. По данному признаку асбест отличается от глинистых минералов, частицы которых в этих средах коагулируют и объединяются в крупные агрегаты, хотя поверхность их также активируется. Происходит химическая деструкция ( аморфи-зация) асбеста. Возникают новые активные центры на внешней и внутренней поверхностях. [35]
Гораздо меньше работ посвящено исследованию степени участия поверхностных групп в адсорбции органических соединений - неэлектролитов или слабых электролитов на углеродных сорбентах. Едсорбируются на окисленных сажах и углях из растворов в гептане сильнее, чем на сажах и углях, освобожденных от окислов прокаливанием при высокой температуре. Увеличение адсорбции они считали следствием взаимодействия л-электронных систем ароматических ядер с сильно протонизированным водородом поверхностных функциональных групп. [36]
При адсорбции молекул фенола полоса валентных колебаний поверхностных групп ОН остается узкой и не исчезает так быстро, как в случае адсорбции анилина и пиридина. [37]
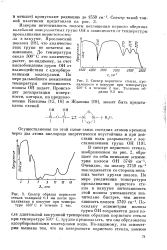 |
Спектр пористого стекла, прокаленного в вакууме при температуре.| Спектр образца пористого стекла толщиной мм после прокаливания в вакууме при температуре 450 С в течение 2 час. [38] |
Измеряя интенсивность полосы поглощения первого обертона колебаний поверхностных групп ОН в зависимости от температуры прокаливания пористого стекла в вакууме, Ярославский показал [18], что количество этих групп не остается неизменным. До температуры около 300 С это количество растет, по-видимому, за счет высвобождения групп ОН от взаимодействия с адсорбированными молекулами. [39]
Своими функциональными группами эти соединения связываются с гидрок-сильными поверхностными группами кремнекислородных олигомеров через водородные связи. Таким образом, полифункциональные органические соединения выполняют функции мостиков, сшивающих молекулы поликремниевой кислоты. [40]
С самого начала предполагалось, что в поверхностных группах должны присутствовать функциональные группы, известные из классической органической химии. [41]
Дейтерообмен позволяет в таких случаях пересчитывать одни лишь поверхностные группы ОН, не затрагивая других поверхностных групп. [42]
Переход мономерной кислоты в раствор способствует полному замещению поверхностных групп сорбента и непрерывно продолжается и на второй стадии процесса. При достаточном значении рН раствора и концентрации сорбируемых ионов концентрация ПКК и ее ионизованной доли возрастает до величины, обеспечивающей насыщение раствора относительно соответствующего гидросиликата. Последующее поступление каждого нового иона SiOf - в раствор вызывает осаждение молекулы MeSi03, которое, естественно, происходит на поверхности продуктов сорбции и представляет собой эпитаксиалыше осаждение силиката. Непрерывное связывание ионов SiO § - и удаление их из раствора вместе с сорбируемыми ионами поддерживает процесс растворения - деполимеризации кремнекислородного остова вплоть до полной перестройки силикагеля в соответствующий гидросиликат. [43]
Примем для простоты, что в этой реакции участвуют поверхностные группы лишь одного типа, а также допустим, что природа группы X одинакова для всех саж. [44]
По-видимому, с ростом рН при увеличении степени диссоциации поверхностных групп происходит эквивалентная адсорбция ионов Ва2 на диссоциированных центрах поверхности. [45]
Страницы: 1 2 3 4