Полярная группа - белок
Cтраница 1
Полярные группы белка будут взаимно связаны в образующейся глобуле и уже не смогут образовывать связей между ними. Следовательно, глобулярные элементы должны растворяться в холодной воде. Это предположение нами было экспериментально проверено. [1]
Водородная связь образуется между полярными группами белка ( - ОН, - NH и NH) и неподеленной электронной парой электроотрицательных элементов ( N, О, S, Р) лекарств, если существуют достаточно благоприятные стерические условия. Это весьма прочная связь, поэтому для ее возникновения не требуется тесного соприкосновения между белками и лекарственными веществами. [2]
С увеличением концентрации спирта в водном растворе уменьшается количество полярных групп белка, присоединяющихся к растворителю. [3]
Основным фактором устойчивости белковых веществ является их гидратация, в которой участвуют как ионизированные, так и полярные группы белка. Первые из них ориентируют диполи воды в электрическом поле, а вторые - взаимодействуют с водой главным образом за счет водородных связей. [4]
Наконец, из химических агентов необходимо упомянуть такие денатурирующие вещества, как ионы тяжелых металлов, также ионы тиоцианата и йода. Эти вещества, по-видимому, образуют довольно прочные соединения с полярными группами белков, искажая систему ионных и водородных связей нативной белковой молекулы. [5]
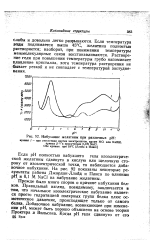 |
Набухание желатины при различных рН. [6] |
Прежде было много споров о причине набухания белков. Правильный взгляд, невидимому, заключается в том, что начальное изоэлектрическое набухание является просто гидратацией полярных групп белка плюс осмотическое давление, происходящее только от самого белка. Добавочное набухание, возникающее при изменении рН, может быть хорошо объяснено на основе теории Проктера и Вильсона. [7]
Основную особенность предложенной модели составляют погруженные в лшшдную матрицу молекулы глобулярного структурного белка, расположенные таким образом, что полярные и ионизированные группы выступают из мембраны в водную среду. Основная масса фос-фолипидов организована в прерывистый жидкостный двойной слой, хотя небольшая доля липидов может специфически взаимодействовать с белками мембран. Заряженные полярные группы белка выступают из мембраны и вместе с гидрофобными участками создают специфический структурный и зарядовый рельеф мембраны. [8]
Устойчивость раствора высокополимеров в полярных растворителях в значительной степени связана с сольватацией полярных групп. Раствор полимера образуется в том случае, если притяжение белка и воды значительно больше взаимного притяжения молекул полимера. Добавление органического растворителя к раствору белка вызывает уменьшение притяжения полярных групп фермента к молекулам воды, так как уменьшается количество молекул воды, присоединяющихся к полярным группам белка. Уменьшение притяжения активных групп фермента к молекулам воды обусловлено главным образом снижением диэлектрической постоянной среды. [9]
Из формулы ( 79) видно, что при высоких концентрациях солей растворимость белка уменьшается пропорционально не только концентрации, но и валентности соли. Однако прямой пропорциональности не существует, так как при увеличении валентности соли в два раза растворимость белка уменьшается более чем в два раза. Осаждающее действие солей высоких концентраций, очевидно, обусловлено конкуренцией между молекулами соли и белка за молекулы растворителя. Не исключено, что в этом случае образуются связи между полярными группами белка и ионами солей, ибо известно, что в осаждении отрицательно заряженных белков играет главную роль положительно заряженный ион соли и наоборот. [10]
Лучший метод - рентгенографический - был применен впервые к гемоглобину. Известно, что кристаллы белков содержат около 50 % кристаллизационной воды. Ее смысл в том, что макромолекулы белка, имеющие неправильную форму, не могут компактно упаковаться друг с другом в про - странственной решетке. Между ними остаются большие зазоры, которые и заполнены растворителем. В эти зазоры ионы солей проникают вполне свободно. Но имеется небольшой объем, недоступный для проникновения ионов электролитов и состоящий из молекул Н20, связанных с полярными группами белка, - это и есть гидратная оболочка в собственном смысле слова. Ее объем был определен Брэггом и Перуцом для гемоглобина путем снятия рентгенограмм в присутствии соли, с-ильно рассеивающей рентгеновские лучи, - йодистого натра. [11]
Страницы: 1