Парциальное давление - аммиак
Cтраница 3
Наличие окиси углерода в растворе при низких температурах почти не влияет на суммарное парциальное давление аммиака, двуокиси углерода и воды над раствором. При повышенных температурах с увеличением концентрации СО парциальное давление двуокиси углерода снижается. [31]
Установлено, что потери азота в процессе получения азотнофосфорного удобрения указанным способом определяются только парциальным давлением аммиака над реакционной смесью или соответственно, степенью гидролиза карбамида. [32]
Установлено, что потери азота в процессе получения азотнофосфорного удобрения указанным способом определяются только парциальным давлением аммиака над реакционной смесью иди соответственно, степенью гидролиза карбамида. [33]
Получение этого уравнения непосредственно из опытов является затруднительным, так как температура слоя и парциальное давление аммиака в данном случае является нерегулируемыми параметрами. [34]
При использовании растворов со степенью карбонизации до 0 54 скорость пропорциональна корню квадратному из парциального давления аммиака над раствором. Последняя величина была измерена и оказалось, что она подчиняется закону Генри. [35]
Процесс основан на том, что при определенном составе поглотительного раствора парциальное давление двуокиси углерода над ним очень мало, а парциальное давление аммиака относительно велико. [36]
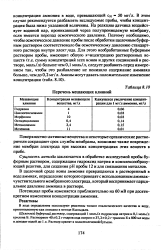 |
Перечень мешающих влияний. [37] |
В щелочной среде ионы аммония превращаются в растворенный в воде аммиак, определение которого проводят с использованием аммиак-чувствительного мембранного электрода, который воспринимает парциальное давление аммиака в растворе. [38]
Распад аммиака на вольфраме при очень низких давлениях ( 0 01 мм) подчиняется тому же уравнению, что и распад на платине, причем скорость распада прямо пропорциональна парциальному давлению аммиака и обратно пропорциональна сумме парциальных давлений водароДа и азота. И здесь при более высоких давлениях азот, практически, не проявляет тормозящего действия. Согласно работе Кенсмана 83, а также более поздней работе Кенсмана, Ламара и Деминга 84, замедляющее действие водорода на распад вообще невелико, но вполне заметно при 950 С; опыты Гиншельвуда и Берка - обнаружили лишь очень незначительное действие или даже отсутствие тормозящего действия водорода при 856 С. [39]
 |
Схема элемента противоточного холодильника труба в трубе. [40] |
Следует заметить, что попытка определить концентрацию NH3 в жидкости абсорбции из состояния насыщения раствора по одному компоненту ( NH3) без учета реальной концентрации другого ( СО2) не имеет смысла даже при равенстве парциального давления аммиака парогазовой фазы и давления паров аммиака над раствором, так как давление NH3 над растворами углеаммонийных солей существенно зависит от степени карбонизации раствора, и одним и тем же составам парогазовой фазы и температуре раствора будут соответствовать совершенно разные концентрации аммиака в растворе, в зависимости от степени его карбонизации. Как было показано ранее, степень карбонизации не является постоянной величиной и определяется всеми факторами, которыми определяется любой процесс абсорбции, в том числе и соотношением расхода фаз. [41]
Применительно к реакции, проводимой под атмосферным давлением, это уравнение можно значительно упростить. Парциальное давление аммиака в этом случае очень невелико ( порядка 0 1 % общего давления), следовательно, второй член уравнения ( 39) можно опустить, так как скорость разложения аммиака очень мала. [42]
Во время работы во всех аппаратах установки устанавливается одинаковое полное давление р 1 4 - 1 6 МПа. Однако парциальные давления аммиака ра и водорода рв, являющиеся слагаемыми полного давления, различны в отдельных аппаратах. [43]
Каким будет парциальное давление аммиака, если полное давление равно 100 атм и если реагенты взяты в стехиометрических количествах. [44]
Поэтому аммиак снижает скорость сероочистки вследствие адсорбции на кислотных точках, на которых перед началом реакции должны адсорбироваться соединения серы. Степень дезактивации пропорциональна парциальному давлению аммиака, поэтому для каждого отдельного объема катализатора необходимо определить предельно допустимую концентрацию аммиака в гидрирующем газе. Для большинства условий работы сероочистных сэндвичей Ай-Си - Ай этот предельный уровень составляет 100 объемы, ч / млн, хотя могут допускаться и более высокие концентрации путем регулирования объемной скорости нафты. Могут допускаться высокие концентрации азота, так как он слабо адсорбируется, а скорость образования аммиака из азота и водорода в условиях сероочистки очень мала. Если осуществляется система рециркуляции газа, то концентрация аммиака постепенно возрастает и может потребоваться отмывка его. [45]
Страницы: 1 2 3 4 5