Высокое парциальное давление - окись - углерод
Cтраница 1
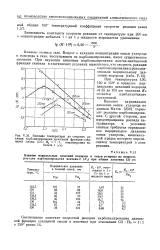 |
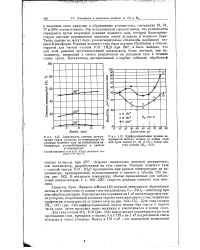
Влияние температуры на скорость реакции карбонилирования дизельной фракции сланцевой смолы ( СО. Н2 1. 1, концентрация кобальта 1 г / л. [1] |
Высокое парциальное давление окиси углерода по данным Натта [258] тормозит реакцию карбонилирования. [2]
Отсюда ясно, что высокое парциальное давление окиси углерода благоприятствует образованию высокомолекулярных соединений. Этот вопрос рассмотрен подробнее в разделе, посвященном механизму синтеза высших спиртов. [3]
Из-за обратимости этих реакций при высоком парциальном давлении окиси углерода концентрация я - и cr - комплексов снижается, что замедляет процесс в таких условиях. [4]
Эти опыты ясно показывают, что гидрогенизация, протекающая в присутствии кобальта при высоких парциальных давлениях окиси углерода, по существу, сводится к гомогенному катализу, в котором роль катализатора играют или [ Со ( СО) 4 ] 2, или НСо ( СО) 4, или оба эти соединения вместе. [5]
Эти исследователи сделали вывод, что углекислота образуется путем вторичной реакции водяного газа, которой благоприятствуют высокие парциальные давления окиси углерода и водяного пара. Такие данные не могут быть удовлетворительно объяснены карбидной теорией Крэксфорда. Реакция водяного газа была изучена Кельбелем и Энгель-гардтом для смесей состава 1СО: Ш20 при 240, и было найдено, что для этой реакции восстановленный катализатор более активен, чем катализатор, введенный в синтез разработкой на исходном газе в течение одних суток. [7]
Из этих данных следует, что при атмосферном давлении термодинамически возможно почти полное превращение этилена ( а также пропилена) в соответствующие оксо-альдегиды. Это вызывается тем обстоятельством, что применение высокого парциального давления окиси углерода предотвращает разложение активного катализатора - гидрокарбонила кобальта. [8]
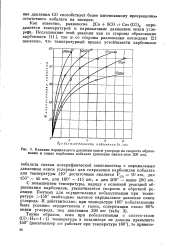 |
Влияние парциального давления окиси углерода на скорость образования и смыва карбонила кобальта ( давление синтез-газа 200 am. [9] |
С повышением температуры, наряду с основной реакцией образования карбонилов, увеличивается скорость и обратной реакции. Поэтому для осуществления кобальтизации при температуре 150 необходимо высокое парциальное давление окиси углерода. [10]
Их стабильность при высоких температурах процесса может быть обеспечена только при высоком парциальном давлении окиси углерода. [11]
Анион Co ( CO) i имеет ту же электронную структуру, что и карбонил никеля. Никель не образует гидрокарбонилов, что может служить объяснением его непригодности в качестве катализатора для гидрирования в условиях высоких парциальных давлений окиси углерода. [12]
Обычно реакцию Гаттермана-Коха проводят, применяя эквимолекулярные количества хлористого алюминия и ароматического углеводорода. Для проведения реакции при атмосферном давлении эту смесь непрерывно насыщают сухим хлористым водородом; желательно также присутствие таких добавок, как полухлористая медь. Высокое парциальное давление окиси углерода ( 30 - 70 am), по-видимому, повышает выход и уменьшает продолжительность реакции, необходимую для получения удовлетворительных результатов. [13]
Другими словами, в этом случае адсорбция под влиянием другого газа скорее повышается, чем уменьшается. Причиной этого, без сомнения, является то, что между адсорбированными молекулами углекислого газа и окиси углерода возникают силы взаимного притяжения, повышающие теплоту адсорбции углекислого газа ( гл. Адсорбция углекислого газа увеличивается подобным образом при наличии высоких парциальных давлений окиси углерода. Другие примеры повышения адсорбции мы обсудим позднее. [14]
Другими словами, в этом случае адсорбция под влиянием другого газа скорее повышается, чем уменьшается. Причиной этого, без сомнения, является то, что между адсорбированными молекулами углекислого газа и окиси углерода возникают силы взаимного притяжения, повышающие теплоту адсорбции углекислого газа ( гл. Адсорбция углекислого газа увеличивается подобным образом при наличии высоких парциальных давлений окиси углерода. [15]
Страницы: 1 2