Диффузия - электролит
Cтраница 4
По существу, кинетическая теория диффузии электролитов рассматривает следствия электрического взаимодействия между зарядами ионов. Электрическое притяжение и отталкивание ионов оказывает некоторое упорядочивающее влияние, действуя против нарушающего порядок теплового движения. Электрическое взаимодействие изменяет статистическое распределение ионов в растворе. Это действие описано в теории Дебая - Хюккеля и развито далее в работах Онзагера, Бьеррума и других, что позволило лучше интерпретировать экспериментальные данные ( см. разд. [46]
Для дальнейшего также существенен случай диффузии электролита Az Xz в растворе. [47]
С увеличением концентрации внешнего раствора усиливается диффузия электролита в фазу ионита. Это приводит к экранированию фиксированного заряда [ R8 ], уменьшению образования пар ионов и увеличению коэффициента активности сорбированного электролита. Когда внешняя концентрация достигает очень высоких значений, эффект Доннана исчезает и свойства внешнего и внутреннего растворов начинают уравниваться. [48]
Таким образом, ионитовая мембрана препятствует диффузии электролитов, но пропускает соответствующие ионы. [49]
В силикатных гелях обнаружена безусло вная диффузия электролитов сквозь их структуры. В своих двух фундаментальных монографиях Лизеганг1 объясняет, например, генезис ритмического образования полос в агатах процессами диффузии. [50]
Опыты показали, что по мере диффузии электролита и кислорода через смазку или по мере разрушения и набухания последней ток все время увеличивается и полярографическая кривая стремится приблизиться к исходной кривой, получаемой на чистом электроде. [51]
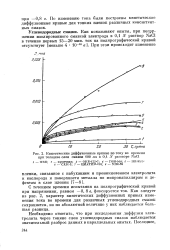 |
Кинетические диффузионные кривые по току во времени при толщине слоя смазки 100 мк в 0 1 N растворе NaCl. [52] |
Необходимо отметить, что при исследовании диффузии электролита через тонкие слои углеводородных смазок наблюдается значительный разброс данных в параллельных опытах. [53]
В общем случае следует допустить возможность диффузии электролита через мембрану. Поэтому за счет различия в подвижностях катиона и аниона и наличия градиента электрохимического потенциала внутри мембраны возникает диффузионный потенциал фдиф. [54]
На основании данных работ по электропроводности и диффузии электролитов в золях и гелях желатины было - сформулировано правильное представление о геле как о системе, представляющей собой своеобразную пространственную сетку, состоящую из структурных непроводящих элементов, между которыми располагается дисперсионная среда. [55]
Это выражение представляет собой уравнение для коэффициента диффузии электролита, диссоциирующего только на два вида ионов. Значение R в этом уравнении должно быть выражено в эргах на градус на моль. [56]
Эф называется эффективным коэффициентом диффузии или коэффициентом диффузии электролита. [57]
Это выражение представляет собой уравнение для коэффициента диффузии электролита, диссоциирующего только на два вида ионов. Значение R в этом уравнении должно быть выражено в эргах на градус на моль. [58]
Важные в теоретическом и практическом аспектах моменты диффузии электролитов рассмотрены в разд. [59]
Страницы: 1 2 3 4