Вторичные алкилгалогениды
Cтраница 2
При использовании бензилхлорида для этого потребовалось меньше 10 мин. Вторичные алкилгалогениды реагируют медленнее - требуется нагревание в течение 2 ч при 110 С. [16]
 |
Карбонилирование галогензамещенных олефинов. [17] |
В жестких условиях кислоты могут быть получены и из насыщенных галогенпроизводных591, Алкилгалогениды образуют карбо-ниевые ионы путем отщепления, галоген-аниона. Однако первичные и вторичные алкилгалогениды малоактивны; только с третичными алкилгалогенидами можно получить приемлемые выходы. [18]
Алкилгалогениды образуют карбо-ниевые ионы путем отщепления галоген-аниона. Однако первичные и вторичные алкилгалогениды малоактивны; только с третичными алкилгалогенидами можно получить приемлемые выходы. [19]
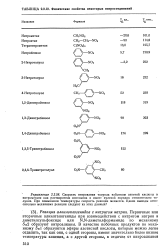 |
Физические свойства некоторых нитросоединений. [20] |
Первичные или вторичные алкилгалогениды при взаимодействии с нитритом натрия в диметилсульфоксиде или М М - диметилформамиде по механизму SN2 образуют нитроалканы. [21]
Исследование механизмов органических реакций вскрывает сходство между различными реакциями. Например, первичные и вторичные алкилгалогениды реагируют с гидроксильными ионами с образованием спирта и галогенид-ионов. [22]
Нитрилы обычно получают из алкилгалогенидов и цианидов натрия или калия. Для этой цели пригодны только первичные и вторичные алкилгалогениды. Третичные алкилгалогениды не образуют нитрилов при взаимодействии с цианид-ионом, а подвергаются элиминированию Е2 с образованием алкенов. [23]
Реакционная способность различных типов алкилгалогенидов рассмотрена выше. Галогенциклоалканы напоминают по своему поведению вторичные алкилгалогениды. Хорошо идет реакция для циклов с пятью и более атомами углерода, в то время как производные циклопропана напоминают винилгалогенид. [24]
Диэфиры малоновой кислоты и ее производных наиболее часто используются в синтезе; их алкилирование - классический подход для образования новых углерод-углеродных связей. Моноалкилирование обычно протекает с умеренным выходом, причем для этого можно применять как первичные, так и вторичные алкилгалогениды. Типичная последовательность реакций представлена на схемах ( 154) [157] и ( 155) [158]; гидролиз малоновых эфиров обсуждается в разд. [25]
В рассмотренной ранее реакции алкенов с галогеноводородами, в соответствии с правилом Марковникова, из несимметричных алкенов образовывались вторичные алкилгалогениды. [26]
В рассмотренной ранее реакции алкенов с галогеноводородами, в соответствии с правилом Марковникова, из несимметричных алке-нов образовывались вторичные алкилгалогениды. [27]
Скорости всех этих реакций уменьшаются в ряду: первичные алкилгалогениды вторичные алкилгалогениды третичные алкилгалогениды. Скорости реакций отщепления галогеноводорода от алкилгалогенидов под действием спиртового раствора КОН с образованием алкена и скорости реакций гидролиза изменяются в обратном порядке: третичные алкилгалогениды вторичные алкилгалогениды первичные алкилгалогениды. [28]
Эта чувствительность синхронных реакций к стерическим эффектам приводит к важным ограничениям при синтезе. Вторичные алкилгалогениды реагируют намного медленнее первичных, и уже в реакциях первичных алкилгалогенидов существуют некоторые стерические ограничения. [30]
Страницы: 1 2 3
