Первичные алкилгалогениды
Cтраница 2
Такая последовательность настолько четко проявляется, что трудно избежать протекания 5 1-реакции для третичных алкилгалогенидов и, наоборот, трудно заставить реагировать по этому механизму первичные алкилгалогениды. [16]
В сухом ацетоне Nal растворяется при комнатной температуре примерно в 20 раз лучше, чем Кг Особой реакциодной способностью обладают сс-галогенкарбонильный соединения, аллил - и бензилгалогениды, причем, бром обменивается легче хлора; первичные алкилгалогениды реагируют легче, чем вторичные и третичные [ 782, 7ЙЗ ], В ароматических соединениях галоген может обмениваться на иод лишь в тощ случае, если связь углерод - галоген ослаблена наличием электронопритягивающил заместителей, например нитрогрупсшй в орто - и ( или) пара-положении. [17]
В качестве алкилирующих агентов в первую очередь применяются алкилгалс гониды, из которых, как известно, наибольшей реакционной способностью обладаю иодиды. Первичные алкилгалогениды реагируют легче, чей вторичные; тротичяы галогениды легко отщепляют галогеноводород под действием ашгаоп и перехода в олефнпы. Вшнилгалогениды более склоним к полимеризации, тогда как аллнлгалс геииды реагируют обычным образом. Реакция а-алкилированиых аллилгалогенидо с аминами почти всегда сопровождается аллильиои перегруппировкой. Полярнц растворители повышают скорость реакции алкилироваиня; чаще всего прлмепяютси вода и этиловый спирт; из-аа более высокой температуры кипения употребляют таюк бензпловый спирт и простые эфиры гликоля. [18]
По своему механизму реакции нуклеофильного замещения делятся на две категории. Первичные алкилгалогениды ( в которых атом галогена связан с первичным атомом углерода) реагируют обычно следующим образом: сначала нуклеофиль-ный реагент подходит к положительно заряженному атому углерода, связанному с атомом галогена, и из двух частиц ( реагента и субстрата) образуется активированный комплекс, который затем распадается на продукт и галогенид-анион. Образование этого комплекса - самый медленный этап реакции и поэтому определяет полную скорость реакции. [19]
Обычно применяют алкилбромиды, реже иодиды и очень редко хлориды. Легче всего реагируют первичные алкилгалогениды, труднее - вторичные, а третичные [ кроме ( CeHs) sCX ] не вступают в реакцию. [20]
Одной из наилучших добавок для этой цели является пиридин. В результате реакции иа олефинов образуются первичные алкилгалогениды через три-алкилалюминий, и эта реакция служит ценным дополнением к реакции присоединения НВг винильной группой в присутствии перекисей. [21]
Мономолекулярный механизм становится предпочтительнее бимолекулярного, когда промежуточный карбока-тион стабилизируется делокализацией электронов и ( или) уменьшением стерического напряжения. Так, в реакциях замещения хлора на гидроксид первичные алкилгалогениды реагируют с гидроксид-анионом по механизму согласованного замещения, а третичные алкилгалогениды-преимущественно по двухста дийному ионизационному механизму. Изменение механизма в этом случае связано как с полярными, так и со стерическими эффектами. Бимолекулярному замещению препятствует большой объем третичной группы и, кроме того, подход атакующего аниона затруднен наличием электроноотталкивающих групп, т.е. реакция бимолекулярного замещения будет нехарактерной для третичных алкил-галогенидов. В то же время ионизационный механизм будет преобладать, когда заряд рассредоточен, т.е. реакционный центр разветвлен; если реакционный центр сдавлен, то образование карбокатиона будет способствовать снятию стерического напряжения. В некоторых случаях карбокатионы стабилизируются резонансом, например трифенилметил-ка-тион, для которого наблюдается только двухстадийный кар-бокатионный механизм. [22]
Поэтому для пространственно затрудненных снегом следует выбирать по возможности такие условия реакции, которые особенно облегчают 5лЛ - тип реакции. Примеры из табл. 26 показывают, что даже первичные алкилгалогениды, которые обычно реагируют исключительно по SN2, вполне удается вытеснить по крайней мере в пограничную область с преобладающим Sivl-характером, если выбрать как можно более полярный и сольватирующий растворитель ( см. также стр. [23]
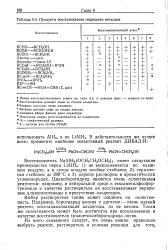 |
Продукты восстановления гидридами металлов. [24] |
Восстановитель NaAlH2 ( OCH2CH2OCH3) 2 имеет следующие преимущества перед LiAlH4: 1) не воспламеняется во влажном воздухе, а в сухом воздухе вообще стабилен; 2) термически стабилен до 200 С и 3) хорошо растворим в ароматических углеводородах. Цианоборогидрид является очень селективным реагентом: например, в нейтральной среде в гексаметилфосфор-триамиде в качестве растворителя он восстанавливает первичные алкилгалогениды в присутствии альдегидов. [25]
Скорости всех этих реакций уменьшаются в ряду: первичные алкилгалогениды вторичные алкилгалогениды третичные алкилгалогениды. Скорости реакций отщепления галогеноводорода от алкилгалогенидов под действием спиртового раствора КОН с образованием алкена и скорости реакций гидролиза изменяются в обратном порядке: третичные алкилгалогениды вторичные алкилгалогениды первичные алкилгалогениды. [26]
Большинство фосфониевых солей получают кватернизацией фосфинов подходящими алкилгалогенидами. Как и в случае обычных 5м2 - реакций, скорость взаимодействия возрастает при переходе от хлоридов к иодидам. Чаще всего используют первичные алкилгалогениды; взаимодействие с низшими галогенидами протекает легко, при увеличении длины алкильной группы скорость реакции уменьшается. Для кватернизации вторичными галогенидами необходимо проводить реакцию в жестких условиях, например, в запаянной трубке при высокой температуре. Полярные растворители, такие, как муравьиная кислота, ДМФ или ацето-нитрил, облегчают реакцию. [27]
Наряду с уходящей группой на соотношение продуктов рсзк ции при нуклеофильном замещении амбидентного аниона больикн влияние оказывает также природа алкильного радикала в субстра те RX. Очевидно, это является следствием изменения механизма реакция а указанном направлении, что, как это изложено в разд. В то время как первичные алкилгалогениды при 5к2 - реакции преимущественно атакуют атом, обладающий высокой поляризуг мостью ( низкой электронной плотностью), третичные алкилгало гениды реагируют в общем по 8м1 - механизму, причем промежуточный хатион преимущественно реагирует с атомом, обладающим наибольшей электронной плотностью ( н-изкой поляризуемостью), так как этот атом в состоянии сильнее электростатически притя нуть образующийся карбокатион. [28]
Каталитическое разложение хлористых алкилов над чистой окисью алюминия сопровождается интенсивной изомеризацией, чего и следовало ожидать, учитывая присутствие хлористого водорода. Например, 1-хлор-к - додекан над этим катализатором при 200 - 250 дает смесь всех шести возможных изомерных н-додеценев приблизительно в равных количествах. Естественно, что нагревание со спиртовым раствором едкой щелочи избавляет от изомеризующего действия свободных кислот, однако в этом случае образуются заметные количества эфиров и первичные алкилгалогениды обычно превращаются в смеси 1 - и 2-олефинов. [29]
Однако этот метод имеет ряд ограничений. Так, галогеналкины нормального строения, содержащие более шести атомов углерода, с трудом реагируют с ацетиленидами металлов. Хлоралкины в этой реакции дают низкие выходы диалкилзамещенных ацетиленов. Вторичные, третичные, а также некоторые первичные алкилгалогениды изостроения в реакции с ацетиленидом натрия отщепляют галогеноводород, Кроме того, в условиях этой реакции ацетиленовые соединения могут подвергаться изомеризации при действии щелочных агентов. [30]
Страницы: 1 2 3