Алкиленкарбонат
Cтраница 2
Показано, что фенолы, в том числе и дифенилолпропан122, при 140 - 200 С реагируют с алкиленкарбонатом ( например, с этиленкарбонатом) в присутствии гидридов щелочных металлов ( лития, натрия, калия); количество катализатора 0 025 - 0 1 о от реакционной массы. [16]
Катализатором служит тетраэтиламмоний-бромид, который получается в виде 10 - 15 % - ного раствора при нагревании в реакторе смеси эквимолярных количеств триэтил-амина и бромистого этила в соответствующем алкиленкарбонате в течение 2 ч при 80 - 100 С. Реакция между окисью этилена и двуокисью углерода проводится под давлением 105 am в течение 20 - 60 мин при определенном температурном режиме. [17]
Целью проекта является разработка научных основ химии и технологии получения разнообразных полифункциональных ароматических и циклических соединений - циклогексанона, циклогексаноноксима, ряда новых сульфохлоридов на основе метил - и галогензамещенных сульфонов, алкиленкарбонатов на основе олефи-нов Сз-Сп, алкларенсульфонатов и белых масел технического и медицинского назначения - новых реактивов, мономеров для синтетических волокон, термостойких пластмасс и материалов специального назначения с использованием хорошо апробированных в промышленности органического синтеза реакций окисления, сульфирования и карбоксилирования. [18]
Алкиленкарбонаты ( в основном этилен - и пропиленкарбонат) производятся в промышленном масштабе в США, ФРГ, Японии. [19]
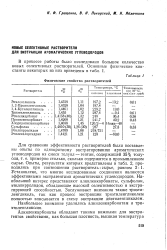 |
Физические свойства растворителей. [20] |
Установлено, что многие исследованные соединения являются эффективными экстрагентами ароматических углеводородов. Наибольший интерес представляют алкиленкарбонаты, сульфолан, этилпирролидон, обладающие высокой селективностью и экстрагирующей способностью. Заслуживает внимания также триэти-ленгликоль, так как процесс экстракции триэтиленгликолем полностью вписывается в схему экстракции дйэтиленгликолем. [21]
Более дешевый и перспективный путь получения алкиленкарбонатов открыт сравнительно недавно. Оказалось, что а-оксиды реагируют с диоксидом углерода с расширением цикла и образованием циклических карбонатов 1 2-гликолей. [22]
Более дешевый и перспективный путь получения алкиленкарбонатов открыт сравнительно недавно. Оказалось, что сс-оксиды реагируют с диоксидом углерода с расширением цикла и образованием циклических карбонатов 1 2-гликолей. [23]
 |
Технологическая схема синтеза алкиленкарбонатов. [24] |
Там при нормальном давлении избыток двуокиси углерода отделяется от жидких продуктов. Кубовый остаток, представляющий собой раствор катализатора в алкиленкарбонате, вновь используется в синтезе. [25]
Исходные вещества непрерывно вводят в аппарат и по мере этого выводят продукты реакции. Такой тип реактора полного смешения подходит для-получения этиленциангидрина или алкиленкарбонатов, где последовательные реакции оксиэтилирования не имеют значения. Однако при синтезе этаноламинов в таком аппарате ухудшается состав продуктов, а при получении неионогенных поверхностно-активных веществ кривая распределения по степени оксиэтилирования становится более пологой по сравнению с изображенной на рис. 79 ( стр. [26]
Наиболее эффективными катализаторами этой реакции являются ионы галогенов ( особенно бромид-ион) в виде солей тетраал-киламмония или щелочных металлов. Реакция протекает под давлением при температуре около 150 С в среде соответствующего алкиленкарбоната и в отличие от других превращений а-окисей является обратимой. [27]
Необходимость длительной операция запаривания волокна при крашении по непрерывной схеме сильно усложняет конструкцию красильной аппаратуры. Для ускорения процесса крашения рекомендуется повысить температуру пропиточного раствора с 40 - 45 С до 100 С и ввести в раствор резорцин или алкиленкарбонаты. Наличие их в красильной ванне приводит к сольватации и дезагрегированию молекул красителя, а также к обратимому набуханию полиакрилонитрильного волокна. При этом резко увеличивается восприимчивость полимера к красителям и улучшается накрашиваемость волокнистого материала. [29]
Реакция протекает под давлением при температуре около 150 С в среде соответствующего алкиленкарбоната и в отличие от других превращений а-окисей является обратимой. Для ее осуществления подходит реактор, изображенный на рис. 79, г ( стр. Накапливающийся при введении а-окиси и СО2 алкиленкарбонат непрерывно выводится из реактора, поступая на перегонку. [30]
Страницы: 1 2 3