Окислительно-восстановительная двойственность
Cтраница 1
Окислительно-восстановительная двойственность присуща системам, содержащим атомы в промежуточных степенях окисления и способных поэтому как отдавать, так и присоединять электроны. [1]
Говоря об окислительно-восстановительной двойственности, не следует забывать, что в некоторых случаях она может быть обусловлена различной природой отдельных составных частей молекулы. [2]
Поэтому HNC2 проявляет окислительно-восстановительную двойственность. [3]
Поэтому НМОг проявляет окислительно-восстановительную двойственность. [4]
Поэтому HNOz проявляет окислительно-восстановительную двойственность. Примерами могут служить следующие реакции. [5]
Поэтому HNO2 проявляет окислительно-восстановительную двойственность. [6]
Поэтому HNOa проявляет окислительно-восстановительную двойственность. [7]
Поэтому HN02 проявляет окислительно-восстановительную двойственность. [8]
Поэтому HN02 проявляет окислительно-восстановительную двойственность. [9]
Поэтому Na2SO3 проявляет окислительно-восстановительную двойственность. [10]
Поэтому HNOz проявляет окислительно-восстановительную двойственность. [11]
Кроме азотистой кислоты окислительно-восстановительной двойственностью обладают сера, иод, пероксид водорода и ряд других веществ. [12]
Кроме азотистой кислоты окислительно-восстановительной двойственностью обладают сера, йод, пероксид водорода и ряд других веществ. [13]
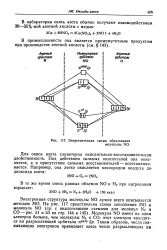 |
Энергетическая схема образования. [14] |
Для окиси азота характерна окислительно-восстановительная двойственность. Под действием сильных окислителей она окисляется, а в присутствии сильных восстановителей - восстанавливается. [15]
Страницы: 1 2 3