Алкилпорфирин
Cтраница 1
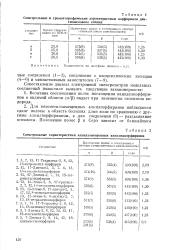 |
Спектральные характеристики алкилзамещенных ванадилпорфиринов. [1] |
Для мезометилзамещенных алкилпорфиринов наблюдается сдвиг полосы в область больших длин волн по сравнению с другими алкилпорфиринами, а для соединения ( 9) - раздваивание сс-полосы. [2]
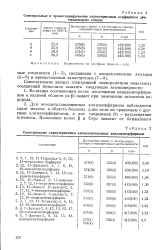 |
Спектральные характеристики алкилзамещенных ванадилпорфиринов. [3] |
Для мезометилзамещенных алкилпорфиринов наблюдается сдвиг полосы в область больших длин волн по сравнению с другими алкилпорфиринами, а для соединения ( 9) - раздваивание а-полосы. [4]
Тенденция преобладания алкилпорфиринов над циклоалканопор-фириновыми структурами по мере погружения продуктивного горизонта и, следовательно, увеличения степени метаморфизма совпадает с известным эффектом метанизации углеводородов с увеличением глубины их залегания. Модельные эксперименты также подтвердили, что в процессе термического и термоокислительного воздействия на нефтяные порфирины относительная доля алкилпорфиринов в них возрастает. [5]
Хроматографическая подвижность близких по молекулярной массе моноциклоалкил - и алкилпорфиринов ( ряды М-2 и М соответственно) связана с их функциональностью. Наряду с увеличением молекулярной массы порфиринов при увеличении их хроматографической подвижности растет и число гомологов каждого ряда, находящихся в данной фракции. Это может быть обусловлено либо меньшими различиями в хроматографической подвижности отдельных представителей порфиринов с высокими молекулярными массами, либо тем, что порфирины каждой массы состоят из нескольких изомеров, количество которых увеличивается при увеличении молекулярной массы. Вполне вероятно, что порфирины с одинаковой молекулярной массой в разных фракциях представлены различными изомерами, отличающимися хроматографической подвижностью. [6]
Предпосылки для успешного применения метода осколочной масс-спектрометрии основаны на способности алкилпорфиринов расщепляться под действием электронного удара по 3-углерод-углеродной связи алкильного заместителя по отношению к пор-финному циклу. При этом наиболее вероятно отщепление фрагмента по р-связи самого массивного алкильного заместителя. Такой процесс приводит к появлению в масс-спектре порфиринов осколочных ионов четной массы, отличающихся от материнских молекулярных ионов на массу отщепившегося алкильного радикала. [7]
Среди порфириновых структур порфиринов с массой меньшей на 6 и 8 единиц, чем масса алкилпорфиринов, содержится незначительное количество. Строение таких соединений, образующих так называемые минорные ряды, точно не установлено. [8]
С увеличением возраста нефти и глубины ее залегания уменьшается суммарное содержание ванадилпорфиринов и увеличивается в них доля алкилпорфиринов. [9]
Немногие единицы процентов содержания приходятся на пор-фириновые структуры с массой на 6 и 8 единиц меньше, чем масса алкилпорфиринов. Строение таких соединений, образующих так называемые минорные ряды, точно не установлено. [10]
Масс-спек-трометрический анализ показал, что в массе ванадилпорфиринов нефти месторождения Прорва содержатся почти одинаковые количества алкил - и моноциклоалкилпорфиринов ( ряды М и М-2), в то время как для ванадилпорфиринов нефти месторождения Прибрежное отмечается преобладание алкилпорфиринов. [11]
Анализ этих соединений методом ВЭЖХ на колонке с обращенной фазой показал, что выявленная ранее общая для ряда органических соединений закономерность в хроматографическом разделении на неполярном сорбенте, заключающаяся в увеличении времени удержания молекулы с ростом числа углеродных атомов в алкильных цепях [2], в случае ванадиловых комплексов алкилпорфиринов не наблюдается. [12]
Тенденция преобладания алкилпорфиринов над циклоалканопор-фириновыми структурами по мере погружения продуктивного горизонта и, следовательно, увеличения степени метаморфизма совпадает с известным эффектом метанизации углеводородов с увеличением глубины их залегания. Модельные эксперименты также подтвердили, что в процессе термического и термоокислительного воздействия на нефтяные порфирины относительная доля алкилпорфиринов в них возрастает. [13]
Электронный спектр синтетического монобензоалкилпорфирина практически полностью идентичен спектру подотипа, наблюдаемого для соединений минорных гомологических рядов. Однако полученное соединение не образует ванадилового комплекса при нагревании в течение нескольких дней с сульфатом вана-дила в различных растворителях, в то время как образование такого комплекса для алкилпорфиринов протекает легко. Невозможность образования ванадиловоЛ комплекса, по-видимому, позволяет исключить монобензоалкшшорфирины из числа возможных структурных аналогов соединений минорных гомологических рядов. [14]
Страницы: 1