Дегидратация - вторичный спирт
Cтраница 1
Дегидратация вторичных спиртов, легко протекающая на глинах, приводит к появлению серии триенов, способных к внутримолекулярной циклизации с образованием ароматического кольца F. Частично при этом происходит отщепление фрагментов алифатической цепи. [1]
При дегидратации вторичных спиртов над MgSO4 наблюдается также большое постоянство энергии активации. Были исследованы спирты: циклогексанол, циклопентанол, пента-нол-2, пропанол-2; их проценты дегидратации при 370 составляли 17 7; 17 8; 18 0; 18 8 и е 15000; 14400; 15200 и 14800 кал / моль соответственно. [3]
При дегидратации алициклических вторичных спиртов количество zjuc - олефина доминирует над транс-изомером и значительно превышает равновесную концентрацию. [4]
При нормальной дегидратации вторичных спиртов с большим выходом образуется тот олефин, который получается путем выделения водорода от более сложного радикала. [5]
Так как дегидратация вторичных спиртов при прочих равных условиях увеличивается с повышением температуры, то целесообразно вести сульфатирование их при возможно более низкой температуре. Консистенция спиртов позволяет проводить сульфатирование при температуре 18 - 20 С. [6]
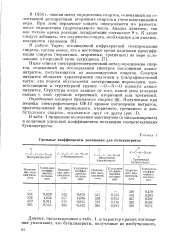 |
Удельные коэффициенты погашения для бутилнитритов. [7] |
В 1958 г. описан метод определения спиртов, основанный на селективной дегидратации вторичных спиртов и учете выделившейся воды. При этом первичные спирты определяются по разности, после определения гидроксильного числа. [8]
Получение ди - emop - алкиловых эфиров часто наталкивается на трудности вследствие дегидратации вторичных спиртов. [9]
Они обычно дегидратируются различными методами, описангыми ниже, а полученные слефины при необходимости гидрируются известными способами до парафинов. При дегидратации несимметричных вторичных спиртов обычно получаются два олефина и может протекать изомеризация двойной связи с образованием более двух олефинов. Но если не происходит структурнш перегруппировки, то при дальнейшем гидрировании, очевидно, получается только один парафин. Если требуется индивидуальный олефин, который не может быть получен из симметричных спиртов или же путем конденсации с аллилгалогенидами, следует обратиться к другим методам, например частичному гидрированию алкилаце-тяленов. В некоторых случаях возможно выделить изомерные олефины при помощи высокоэффективной фракционированной перегонки. [10]
Фрейдлин с сотрудниками [276] при исследовании реакций дегидратации вторичных спиртов. В продуктах дегидратации пентанола-2 и пентанола-3 преобладали пентены-2, а пен-тена-1 было очень мало. Но особенность реакции дегидратации вторичных спиртов заключается в том, что реакция протекает стереоспецифично в направлении образования термодинамически менее устойчивых цис-изомеров. [11]
Вторичные спирты реагируют с серной кислотой по механизмам, пограничным между SN2 и SN. Получение ди-ютгор-алкиловых эфиров часто наталкивается на трудности вследствие дегидратации вторичных спиртов. [12]
При 250 - 300 С основные органические кислоты декарбоксилнруются, образуя углеводороды, по числу атомов углерода на один меньше го сравнению с исходной кислотой. Спирты превращаются в соответствующие олефины, причем при дегидратации вторичных спиртов могут образоваться два олефина. [13]
Между тем было показано, что в ряду циклоалканов реакции дегидратации вторичных спиртов в кислой среде и дезамини-рования аминов азотистой кислотой ( реакции, мономолекулярный механизм которых достоверно доказан) приводят преимущественно к получению этиленовых углеводородов, образующихся в результате транс-отщепления. [14]
Для одноатомных спиртов легкость дегидратации различна; спирты по их способности к дегидратации можно расположить в следующий ряд: третичные вторичные первичные. Так, если в качестве дегидратирующего агента использовать серную кислоту, то требуется меньшая концентрация и ( или) более низкая температура для третичных спиртов по сравнению со вторичными, и аналогичным образом дегидратацию вторичных спиртов следует проводить в более мягких условиях, чем первичных спиртов. [15]
Страницы: 1 2
