Дегидрирование - боковая цепь
Cтраница 1
Дегидрирование боковых цепей является важным методом получения реакционноспособных промежуточных веществ для синтеза многих органических соединений. Простейшим примером может служить получение стирола из этилбензола. Методика приготовления этого катализатора была описана выше. Как следует из данных, приведенных в табл. 17 [300, 301], реакция при постоянной объемной скорости исходных веществ чувствительна к давлению и температуре. Приведенные данные характеризуют 30-минутный период реакции; уголь, накапливающийся за это время на поверхности катализатора, сжигают, после чего процесс можно вести вновь. [1]
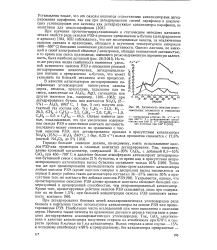 |
Активность окислов редко. [2] |
При дегидрировании боковых цепей алкилароматических углеводородов ряда бензола и нафталина также используются катализаторы на основе РЗЭ или промотированные РЗЭ. Наибольшее число исследований при этом выполнено с окислами церия. Имеются также патенты на применение двуокиси церия в чистом виде в реакциях дегидрирования алкилароматических углеводородов. Так, СеО2 запатентована в качестве катализатора получения стирола из этилбензола при 670 С и скорости протока 8 мл / мин на 1 мл катализатора. [3]
Отличием реакций дегидрирования боковых цепей от дегидрирования парафиновых углеводородов является легкость их осуществления на ряде катализаторов с избирательностью до 95 % благодаря сопряжению СС-связи в образующемся алкенильном производном с ароматическим кольцом. [4]
В реакциях дегидрирования боковых цепей алкилароматических углеводородов окислы элементов подгруппы титана также используются в основном в составе сложных катализаторов. При этом большей частью их роль не удается установить. Согласно [121], ТЮ2 и ZrO2 относятся к группе добавок, влияющих на активность без существенного изменения избирательности процесса. Сложный циркониевый катализатор дегидрирования олефинов ( бутена в бутадиен) [ 119] активен и в реакциях дегидрирования боковых цепей алкилароматических углеводородов. [5]
В катализе дегидрирования боковых цепей ароматических углеводородов окислы ванадия низшей валентности находят весьма ограниченное применение. [6]
Имеются экспериментальные подтверждения возможности дегидрирования боковой цепи алкилтиофенов. В патентах [544, 545] приводятся данные о протекании этой реакции при 400 - 600 в присутствии окислов металлов, в частности окиси хрома на боксите. [7]
Сульфиды металлов ускоряют главным образом реакции дегидрирования боковой цепи алкилтиофена и его разложения с выделением сероводорода. Кинетические исследования показывают, что эти реакции протекают независимо и подчиняются уравнению первого порядка. [8]
В литературе имеются немногочисленные данные о дегидрировании боковых цепей алкилароматических углеводородов под влиянием трехокиси молибдена и окислов урана. [9]
Для элементов рассматриваемой группы также малохарактерны и процессы дегидрирования боковых цепей алкилароматических углеводородов. В патенте [94] указывается, что в присутствии активированного угля дегидрирование этилбензола или этилнафталина в соответствующие винильные производные протекает при 650 С, в то время как для дегидрирования этих углеводородов в отсутствие угля требуется температура 850 - 1200 С. [10]
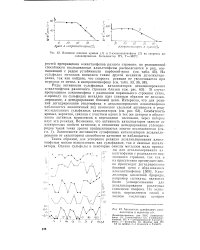 |
Взаимное влияние кумола ( 1 и 2-изопропилтиофена ( 2 на скорость дезалкилирования. Катализатор HY, Г 300 С.| Активность сульфидных катализаторов и величины е / г. [11] |
В случае превращения алкилтиофена с радикалом нормального строения ( этил, н-пропил) на сульфидах металлов идет главным образом не дезалки-лирование, а дегидрирование боковой цепи. Симбатность кривых, вероятно, связана с участием одних и тех же центров в образовании активных комплексов в переходном состоянии, через которое идут эти реакции. Возможно, что активность катализаторов зависит от электронных свойств катионов; в отношении дегидрирования углеводородов такой точки зрения придерживаются многие исследователи ( см. гл. Зависимости активности сульфидных катализаторов дезалкилирования от акцепторной способности катионов не наблюдается. [12]
В отличие от этилбензола гетероциклический МЭП в условиях реакции является менее стабильным. Помимо деструкции пиридинового кольца и дегидрирования боковых цепей одновременно протекают реакции деалкилирования и алкилирования. В катализате обнаружены такие побочные продукты, как пиридин, 2 - и 3-пико-лины, 2 5-лутидин, 3-этилпиридин, 3-винилпиридин, 2 - ЭТИЛ-5-ВИ-нилпиридин, 2-винил - 5-этилпиридин, 2 5-дивинилпиридин и др. Наличие в катализате дивинилпиридина даже в незначительных количествах ведет к большим осложнениям в процессе выделения МВП из печного масла, так как он вызывает образование губчатого полимера в ректификационных колоннах. [13]
В виде индивидуального соединения окись алюминия в качестве катализатора дегидрирования боковых цепей применяется сравнительно редко. [14]
В настоящей главе делается попытка восполнить этот пробел; наряду с описанием окиснохромовых катализаторов приведены, по возможности, подробные сведения о влиянии на процессы дегидрирования других контактов. Из-за огромного количества литературного материала, касающегося реакций каталитического дегидрирования углеводородов, в качестве объектов исследования рассматриваются реакции каталитического дегидрирования парафинов и олефинов С2 - С5 в соответствующие олефины и диолефины, а также дегидрирования боковых цепей алки-лароматических соединений. [15]
Страницы: 1 2