Дегидрогенизация - изобутан
Cтраница 1
Дегидрогенизация изобутана в изо-бутилен или бутана в бутилен; температура 480 - 550, время контактирования 3 - 20 сек. [1]
По-видимому, производство изобутилена дегидрогенизацией изобутана более экономично, чем получение его из изобутилового спирта. [2]
Точно таким же путем при дегидрогенизации изобутана получается изобутилен. Если каталитическая дегидрогенизация изобутана проводится при пониженных температурах ( 350 - 450), то образующийся при этом продукт не содержит примесей изомеров с прямой цепью, от которых он трудно отделяется. [3]
Однако при сернокислотном алкилировании и сочетании его с изомеризацией н-бутана и дегидрогенизацией изобутана получение алкилата и получение изооктана одинаково выгодны в отношении использования всего сырья. [4]
Естественно, что эта задача должна быть решена на основе выходов при изомеризации бутана и дегидрогенизации изобутана. [5]
Естественно, что при решении этой задачи нужно исходить из значений выходов при изомеризации бутана и дегидрогенизации изобутана. [6]
В промышленности применяется изобутилен, полученный из заводских газов, из природных газов при изомеризации и-бутана и при дегидрогенизации изобутана. [7]
По данным Хэрда и Спенса [60], Пиза [102], Фрея и Хэппа [36] Марека и Нейгауза [93] и Шультца и Веллера [120] дегидрогенизация изобутана в изобутилен и водород занимает такое же место, как и расщепление на пропилен и метан, или, возможно, даже большее. Марек и Неигауз путем экстраполяции к нулевому значению времени подсчитали, что при 600 - 650 С первичное расщепление изобутана дает 63 % мол. Шультц и Веллер нашли, что при 700 С первичный крекинг изобутана дает 52 % мол. [8]
Эглофф, Томас и Линн [28] изучали влияние давления на разложение бутанов и пропана. Наоборот, дегидрогенизация изобутана резко уменьшается с повышением давления. Эти результаты вполне согласуются с обратимостью реакции дегидрогенизации простых парафинов и фактической необратимостью реакций расщепления. [9]
Для производства бутилкаучука и полиизобутилена необходимо большое количество изобутена. Поскольку из газов крекинга нельзя получить достаточного количества изобутена, прибегают к дегидрогенизации изобутана природных или заводских газов. [10]
Естественно, что эта задача должна быть решена на основе выходов при изомеризации бутана и дегидрогенизации изобутана. [11]
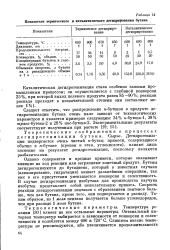 |
Показатели термического и каталитического дегидрирования бутана. [12] |
Однако содержатся и вредные примеси, которые оказывают влияние на ход реакции или загрязняют конечный продукт. Бутены дегидрогенизуются до бутадиена, который в известных случаях ( алкилирование, гидратация) мешает дальнейшим операциям, так как в его присутствии уменьшается конверсия и селективность. В случае дегидрогенизации изобутана для производства каучука изобутен представляет собой нежелательную примесь. Скорость реакции дегидрогенизации пентанов с образованием пентенов больше, чем для бутана, кроме того, они подвергаются и распаду. Таким образом, из 1 моля пентана получается больше углеводородов, чем при распаде 1 моля бутана. [13]
Результаты хроматографического анализа продуктов крекинга ( табл. 23 и 24) показывают, что при 20 мм ( 548) вначале изобутан распадается быстрее ( за первую минуту), чем бутан. При более высокой температуре ( 573) наблюдается обратное - изобутан при значительном времени крекинга распадается медленнее, чем бутан. Крекинг бутана на метан и пропилен в этих, условиях более чем в пять раз, а на этан и этилен более чем в два раза превосходит дегидрогенизацию. В тех же условиях дегидрогенизация изобутана в 7 раз, а деметанизация его в три раза превосходят деэтанизацию. [14]
Страницы: 1