Деградация - полисахарид
Cтраница 1
Деградация полисахаридов начинается на ранних стадиях процесса, однако некоторая часть полисахаридов может сохраняться многие миллионы лет. [1]
В меньшей форме деградация полисахаридов выражена в образце № 1 также Южноуральского бассейна, но другого месторождения. [2]
Ниже даны три примера деградации полисахаридов, в которых олигосахариды защищают от дальнейшего гидролиза искусственными методами. Первый пример - это гидролиз инулина растворимой в воде полисти-ролсульфокислотой, проводимый внутри целлофановой трубки. [3]
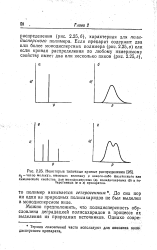 |
Некоторые типичные кривые распределения. щ - число молекул, имеющих величину р какого-либо физического или. [4] |
Можно предположить, что подидисперсность обусловлена деградацией полисахаридов в процессе их выделения из природных источников. [5]
Сам процесс щелочной экстракции гемицеллюлоз из холоцеллюлозы сопровождается деградацией полисахаридов и увеличением в них содержания карбоксильных и карбонильных групп. Полагают [6], что в этом случае могут происходить четыре типа реакций: 1) отщепление ацетильных групп от частично ацетили-рованных полисахаридов, 2) деградация, обусловленная наличием редуцирующих групп, 3) щелочной гидролиз глюкозидных связей, 4) разрыв химических связей между гемицеллюлозами и другими компонентами клеточной стенки. Эти реакции приводят к химическому изменению гемицеллюлоз. Поэтому необходимо соблюдать большую осторожность как при предварительной обработке древесины, так и в процессе извлечения гемицеллюлоз щелочью. [6]
В процессе получения ячменного солода и при прорастании семян происходит общая ферментативная деградация полисахаридов, отличных от крахмала. В ячмене присутствуют уже отмеченная эндо-р-глюкозаназа, экзо-р-глюкозаназа и целлобиаза. [7]
Применяя метод метилирования для исследования строения молекул полисахаридов, необходимо учитывать следующее: в процессе метилирования при использовании щелочных растворов может происходить частичная деградация полисахаридов, окисление, а также отщепление некоторых функциональных групп, например ацетильных групп, метоксильных групп, связанных сложноэфирной связью с карбоксильными группами уроновых кислот. Таким образом, в результате метилирования не всегда получают полисахарид в химически неизмененном виде. [8]
Поведение полисахаридов древесины при повышенных температурах в щелочной среде существенно отличается из-за появления принципиально иного механизма их деструкции, приводящего к отщеплению редуцирующих концевых звеньев, т.е. к деполимеризации, тогда как в кислой среде происходит только деградация полисахаридов. В щелочной среде деструкция полисахаридов древесины происходит в результате трех процессов: деполимеризации, щелочного гидролиза и окислительной деструкции. Последняя обусловлена остаточным кислородом, неизбежно присутствующим как в реакционной среде, так и в пористой структуре древесины. [9]
Каждый метод имеет свои недостатки. Так, методы, основанные на диспергировании крахмала в кислой среде и последующем измерении оптического вращения раствора или получении иод-крахмального комплекса, по-видимому, вызывают слишком глубокую деградацию полисахаридов, что приводит либо к несоответствию между величиной оптического вращения и содержанием полисахаридов, либо к образованию осаждающихся декстринов, не содержащих иода. Более того, кислотный гидролиз сложных крахмалсодержащих продуктов может сопровождаться деградацией некоторых компонентов клеточной стенки ( пектиновых веществ, гемицеллюлоз) и появлением восстанавливающих моно - и олигосахаридов. [10]
Определение содержания лигнина имеет важное значение в анализе древесины и для характеристики технических целлюлоз. Методы количественного определения лигнина подразделяют на прямые методы, в которых лигнин определяют в виде остатка, и косвенные. В косвенных методах содержание лигнина рассчитывают по разности после нахождения полисахаридов, определяют спектро-фотометрическими методами или по реакциям с окислителями. Для всех методов характерны трудности, обусловленные влиянием других веществ ( экстрактивных, продуктов деградации полисахаридов), а также сомнениями в полноте установления количества лигнина. [11]
ИК-спектры образцов древесины указывают на присутствие конденсированных ароматических колец, образовавшихся главным образом из лигнина. С увеличением возраста превращение лигнина в конденсированные ароматические системы усиливается. Битуминозный уголь имеет высокое содержание таких систем. В конце этого процесса получается графит - кристаллическая модификация углерода с гексагональной структурой, в которой атомы углерода образуют слои, расположенные друг над другом. Ароматические кольца могут возникать и из продуктов деградации полисахаридов. [12]
Истинные грибы, Fungi - наземные организмы, мицелий которых сходен с мицелием прокариотных стрептомицетов и представлен длинными ветвящимися гифами - трубками со сложенной хитином оболочкой. Мицелий составляет один большой организм. Несмотря на то, что грибы относят к микроорганизмам, они на самом деле представляют, формально говоря, самые крупные организмы на Земле. Мицелий грибов приспособлен для развития в почве и способен переносить контакт с воздухом, нередко образуя воздушный мицелий; поэтому грибы выигрывают у бактерий при переходе к засушливым ( ксерофитным) условиям. Сеть мицелия обеспечивает возможность транспорта по ней питательных веществ от клетки к клетке. Вместе с тем грибы обладают мощным аппаратом гидролитических экзоферментов, обеспечивающих им возможность деградации полисахаридов растительных оболочек ( и, что особенно важно, лигнина), липидов, нерастворимых азотистых соединений. Они составляют группу сапрофитных микроми-цетов, особенно богатых в лесной подстилке. Многие грибы вступают в симбиотические и паразитические отношения с сосудистыми растениями, так что их можно рассматривать как постоянные компоненты растительно-грибной системы. [13]
Страницы: 1