Алкилфурана
Cтраница 1
Алкилфураны легко могут быть получены замыканием цикла ( см. разд. Гриньяра, сопровождающимися дальнейшими превращениями, а также алкилированием фуранов ( см. разд. Используют также восстановление альдегидов и кетонов ряда фурана по реакции Кижнера - Вольфа. [1]
Алкилфураны замещаются главным образом по положению 2 [24]; 2 5-диалкилфураны могут быть проацилированы по р-положению, хотя обычно с большим трудом. [2]
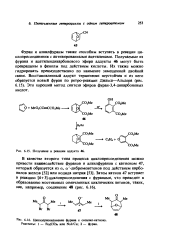 |
Получение и реакции аддукта 46. [3] |
Фуран и алкилфураны также способны вступать в реакции ци-клоприсоединения с активированными ацетиленами. Получаемые из фурана и ацетилендикарбонового эфира аддукты 46 могут быть превращены в фенолы под действием кислоты. [4]
Сам фуран и простые алкилфураны относительно устойчивы к действию водных растворов минеральных кислот, однако фуран мгновенно разлагается под действием концентрированной серной кислоты или кислот Льюиса, например хлорида алюминия. Фуран медленно реагирует с хлороводородом либо в концентрированного водного раствора, либо в растворителе, не гидроксильных групп. [5]
В кислой среде алкилфураны легко претерпевают раскрытие кольца с образованием 1 4-дикетонов ( процесс, обратный синтезу Пааля - Кнорра; см. разд. Фураны с электроноакцепторными заместителями обычно устойчивы к действию кислот. [6]
Каталитическое восстановление ал-кнлфурилкар бинолов в алкилфураны. [7]
В качестве разделяющих агентов могут применяться ароматические углеводороды [325, 326], фуран и алкилфураны [327], тетрагидрофуран к - его производные [328, 329], нитрилы [330] и другие вещества, обладающие малой взаимной растворимостью с водой и обра - 5ующие с ней гетероазеотрошы. Желательно применение таких веществ, которые образуют гетероазеотропы только с водой я е дают тройных азеотропов с водой и веществом, подвергаемым обезвоживанию. [8]
Для фурана не удается провести ни реакцию Манниха ( MezNH, ШСО, Н), ни азосочетание, что свидетельствует о более низкой реакционной способности фурана по сравнению с пирролом, хотя алкилфураны со свободными положениями 2 и 5 вступают в реакцию Манниха. [9]
Метод азеотропной ректификации получил широкое применение для обезвоживания не только спиртов, но и других соединений, например, кетонов, эфиров, кислот и др. В качестве разделяющих агентов могут применяться ароматические углеводороды [325, 326], фуран и алкилфураны [327], тетрагидрофуран и его производные [328, 329], нитрилы [330] и другие вещества, обладающие малой взаимной растворимостью с водой и образующие с ней гетероазеотропы. Желательно применение таких веществ, которые образуют гетероазеотропы только с водой и не дают тройных азеотропов с водой и веществом, подвергаемым обезвоживанию. [10]
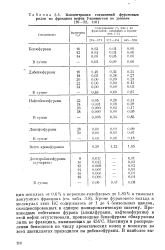 |
Концентрация соединений фурановых рядов во фракциях нефти Уилмингтон по данным. [11] |
Производные собственно фурана ( алкилфураны, нафтенофураны) в этой нефти отсутствовали, производные бензофурана обнаружены лишь во фракциях, выкипающих до 454 С. Максимум в распределении бензологов по числу ароматических колец в молекуле во всех дистиллятах приходился на дибензофураны. [12]
Обработка фуранов бромом и ацетатом натрия в метаноле приводит к тем же продуктам. При электрохимическом ацетоксилировании фурана в уксусной кислоте образуются цис - и гранс-2 5-диацетокси - 2 5-дигидрофу-раны ( 12 %), однако алкилфураны дают продукты ацетоксилиро-вания боковой цепи. [13]
Страницы: 1