Буферное действие
Cтраница 2
Оптимальное буферное действие имеет раствор, в котором кислота и основание находятся в эквимолярном отношении 1: 1, так как при этом изменение рН минимально при добавлении как сильной кислоты, так и сильного основания. [16]
 |
Некоторые буферные смеси и формулы для расчета концентраций иона Н3О и рН. [17] |
Буферное действие растворов имеет важное значение в практике химического анализа, поэтому нужно знать широко применяемые буферные смеси и уметь вычислить рН таких растворов. [18]
Буферное действие белков плазмы сравнительно с бикарбонатами невелико. Буферные свойства гемоглобина обусловлены возможностью взаимодействия кисло реагирующих соединений с калиевой солью гемоглобина с образованием эквивалентного количества соответствующей калийной соли и свободного гемоглобина ( НЬ), обладающего характером очень слабой органической кислоты. [19]
 |
Ощупывание поверхности профилометром. [20] |
Подобное высокое буферное действие, или грузоподъемность, масляной пленки лежит в основе другого явления, исследованного Е. Ф. Пичугиным и автором. Многие приборы позволяют оценивать микрошероховатость твердой поверхности, например стали, если проводить по поверхности АА алмазным или другим твердым острием С ( рис. 89), связанным с прибором, регистрирующим вертикальные перемещения острия, совершаемые им при огибании микровыстуцов поверхности. [21]
 |
Изменение коэффициента трения в зависимости от температурного режима работы подшипника. [22] |
Буферное действие углеродистых примесей обусловлено тем, что размеры частиц основной массы соизмеримы с толщиной масляной пленки ( около 1 мкм) в условиях граничной смазки и высотой микронеровностей таких пар трения, как шейка и подшипник коленчатого вала, цилиндр и юбка поршня и поршневые кольца. [23]
Буферное действие подобных смесей основано на следующих процессах. [24]
Количественно буферное действие раствора по Ван-Слайку ( 1922 г.) выражается его буферной емкостью. [25]
Буферное действие подобных смесей основано на следующем. [26]
Буферное действие ацетатной смеси заключается в следующем. [27]
Буферное действие растворов индивидуальных солей объясняется возникновением в процессе гидролиза кислот и оснований. [28]
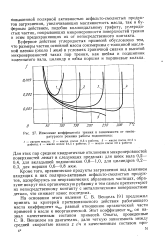
Буферное действие сильных и слабых кислот и сильных оснований представлено на рис. V. Прежде всего очевидно, что сильные кислоты и основания имеют большую буферность, чем слабокислые буферные растворы той же концентрации. Кроме того, максимум буферной емкости ацетатной, фталатной, фосфатной и боратной систем примерно таков, как это предсказывает уравнение (V.15), а именно: 0 028 для 0 05 М систем, 0 057 для 0 1 М систем и 0 115 для 0 2 М систем. [29]
Буферным действием должны также обладать смеси кислых солей разной основности, например NaH2PO4 Na2HPO4, где первая соль играет роль слабой кислоты, а вторая-ее соли. [30]
Страницы: 1 2 3 4