Пассивирующее действие - кислород
Cтраница 1
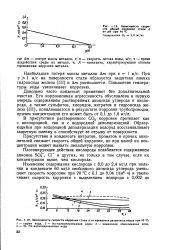 |
Зависимость скорости общей коррозии стали k от рН при 40 С. [1] |
Пассивирующее действие кислорода ослабляется содержанием анионов S042, СГ и других, но только в том случае, если их концентрация выше, чем кислорода. [2]
Пассивирующее действие кислорода и других окислителей существенно зависит от активирующих свойств анионов С1, S02 и др. Если концентрация этих анионов больше, чем концентрация пассиваторов, например кислорода, пассивация металла затрудняется. По данным работы [47], подобное явление связано с конкурирующей адсорбцией. Установлено, что ионы О - и S042 -, а также другие компоненты принимают непосредственное участие в первоначальной стадии анодного процесса перехода металла в раствор. При этом они образуют комплексы металла с анионами. [3]
Пассивирующее действие кислорода тормозит развитие коррозии стали. Пассивность металла - повышенная коррозионная его стойкость, вызванная торможением анодного процесса. [4]
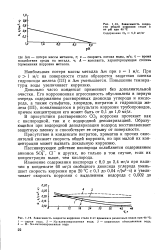 |
Зависимость скорости общей коррозии стали от рН при 40 С.| Зависимость скорости коррозии стали от времени в различных водах при 40 С. [5] |
Пассивирующее действие кислорода ослабляется содержанием анионов SOf, Cl - и других, но только в том случае, если их концентрация выше, чем кислорода. [6]
По-видимому, в условиях атмосферной коррозии при свободном доступе кислорода совместное пассивирующее действие кислорода и хромат-иона способно подавить агрессивное действие амина, что и обеспечивает защиту изделий из сочетания черного и цветного металлов. [7]
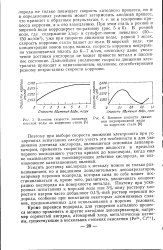 |
Влияние скорости движения морской воды на коррозию стали 5 ].| Влияние скорости движения водопроводной воды на коррозию стали. [8] |
Поэтому при выборе скорости движения электролита при ускоренных испытаниях следует учесть эти особенности и для увеличения доставки кислорода, являющегося основным деполяризатором, применять скорости движения жидкости в пределах первого восходящего участка кривых до максимума, когда еще не сказываются ни пассивирующее действие кислорода, ни возникновение кавитационных явлений. [9]
Таким образом, ускоряющее действие анионов, например галоид-ионов, на растворение металла осуществляется двумя путями: во-первых, они образуют на поверхности с металлом адсорбированный комплекс, который легко теряет связь с основной массой металла и переходит в раствор; во-вторых, они устраняют пассивирующее действие кислорода, адсорбционно вытесняя его с поверхности металла. Замедляющее действие атомов ( тех же галоидов) связано с образованием прочных химических поверхностных соединений. [10]
Таким образом, ускоряющее действие анионов, например галоид-ионов, на растворение металлов осуществляется двумя путями: во-первых, они образуют на поверхности с металлом адсорбированный комплекс, который легко теряет связь с основной массой металла и переходит в раствор; во-вторых, они устраняют пассивирующее действие кислорода, адсорбционно вытесняя его с поверхности ме-талла. Замедляющее действие атомов, например тех же галоидов, связывается с образованием прочных химических поверхностных соединении. [11]
Это обусловлено двойственным характером анодной поляризации. Любое смещение потенциала за стационарлые значения увеличивает, с одной стороны, степень окисления поверхности, что затрудняет активирование поверхности стали хлор-ионом, и, с другой, облегчает адсорбцию хлор-ионов, а стало быть, и вытеснение ими кислорода. При малых плотностях тока преобладает пассивирующее действие кислорода, и поэтому хлор-ионы не могут активировать металл, несмотря на то, что потенциал намного положительнее потенциала питтингообразования. [12]
Это обусловлено двойственным характером анодной поляризации. Любое смещение потенциала за стационардые значения увеличивает, с одной стороны, степень окисления поверхности, что затрудняет активирование поверхности стали хлор-ионом, и, с другой, облегчает адсорбцию хлор-ионов, а стало быть, и вытеснение ими кислорода. При малых плотностях тока преобладает пассивирующее действие кислорода, и поэтому хлор-ионы не могут активировать металл, несмотря на то, что потенциал намного положительнее потенциала питтингообразования. [13]
Кривая, приведенная на рис. 111 - 14, показывает связь между коррозией металла и концентрацией растворенного в воде кислорода. Скорость коррозии углеродистой стали возрастает пропорционально увеличению до определенного значения концентрации растворенного в воде кислорода. После достижения этого значения концентрации кислорода наступает резкое снижение скорости коррозии, вызванное пассивирующим действием кислорода. Если в воде имеются хлор-ионы, то достижение пассивного состояния затруднено, а в некоторых случаях даже невозможно. [14]
Таким образом, с увеличением концентрации кислорода в растворе усиливается пассивирование поверхности золота, следствием чего является сильное анодное торможение процесса растворения. Однако при анализе этих кривых нужно учитывать влияние обоих компонентов реакции - цианида и кислорода - на процесс пассивирования. Торможение растворения при смещении стационарного потенциала в положительную сторону в растворах с повышенной концентрацией кислорода и ослабление пассивирующего действия кислорода при повышении концентрации цианида можно, вероятно, объяснить исходя из представления о промежуточном адсорбционном характере взаимодействия кислорода и цианида с поверхностью золота. [15]
Страницы: 1 2