Кооперативное действие
Cтраница 3
Хотя активный центр относительно невелик, он должен все же представлять собой довольно сложную структуру. Известно, что он определяет и каталитическую активность, и специфичность, а поэтому должен обеспечить весьма тесное взаимодействие, точное в пространственном ( геометрическом) и химическом отношении с молекулами субстрата или с их необходимыми частями. Для проявления активности этого центра необходима его трехмерная структура, кооперативное действие его различных участков, возникающее при их топографическом сближении и соответствующей ориентации. Следовательно, необходима определенная трехмерная структура всей молекулы фермента. В настоящее время принято считать, что активный центр не располагается в пределах какого-либо небольшого отрезка одной пептидной цепи, а представляет совокупность групп, расположенных на двух или нескольких цепях или на различных участках одной, но сложно изогнутой пептидной цепи. Нейратом ( рис, 12), На модели черными линиями показан активный центр химотрипсина, который занимает небольшую область и включает два остатка гистидина и один остаток серина. Здесь имеется одна единственная пептидная цепь, изогнутая таким образом, что различные участки ее ( различные аминокислотные остатки) сближены и образуют каталитически активный центр. Ясно, что каталитическая способность химотрипсина зависит не только от наличия тех или иных функциональных групп, но главным образом от конфигурации всей макроструктуры белка, поскольку эта конфигурация определяет взаимное расположение групп активного центра. Отсюда ясно и значение стабильности макроструктуры ( третичной структуры) белка для выявления и сохранения ферментативной активности. [31]
Именно такое расположение имеется в активном центре фосфо-глюкомутазы, где серии связан с остатком имидазола. Если же имидазола рядом нет, то он может приблизиться к серину, находясь в соседней пептидной цепи или в отдельном участке той же цепи, при соответствующем ее изгибе. Можно представить себе, например, такой механизм реакций: сложный эфир серина, который образуется в качестве промежуточного продукта, подвергается гидролизу благодаря каталитическому действию близлежащего имидазольного радикала. Для такого кооперативного действия соседних групп нужна точно определенная конформация пептидных цепей в участках, формирующих активный центр. Флуктуации зарядов в молекуле ферментного белка могут вызывать некоторые изгибы цепей около имидазольных остатков, влияя тем самым на их активность. Вероятно, аналогично осуществляется перенос фосфатных остатков при действии фосфоглюкомутазы. Вначале образуется фосфорилированный фермент, после чего в результате гидролиза освобождается фосфатная группа. [32]
Данные о свойствах и распространенности природных цеолитов позволяют рассматривать цеолитовые породы с содержанием полезного компонента более 50 % как новый тип минерального сырья многоцелевого использования. Высокие содержания цеолитов в рудах, практически неисчерпаемые запасы и уникальные ионообменные и адсорбционные свойства определяют широкие возможности использования природных цеолитов в промышленности и сельском хозяйстве. Особенности вторичной пористой структуры цеолитизированных туфов определяют важные явления неспецифической сорбции крупных молекул, а также высокую влагоем-кость, значительно превышающую содержание цеолитовой воды. Таким образом, свойства цеолитизированных туфов определяются кооперативным действием таких факторов, как содержание, вид и состав цеолитов и сопутствующих минералов, размер микрокристаллитов, а также вторичная пористость, связанная со специфической микродрузовой текстурой пород. [33]
Специфичность гликопротеинов и гликолипидов определяется размером и формой гетеросахаридных концевых цепей, окруженных водной средой с внешней стороны мембраны. Разные последовательности углеводных остатков и различные типы связи между ними создают большое многообразие гетеросахаридных цепей, даже если полисахарид состоит всего из нескольких типов углеводных остатков. Такое многообразие усиливается не-ковалентными взаимодействиями моносахаридных остатков с соседними гетеросахаридными белками. Эти взаимодействия приводят к образованию комплексов на поверхности мембраны и их кооперативному действию. [34]
Любая поправка на отклонение от сферичности иэ-аа шероховатости поверхности раздела или асимметрии ядра должна уменьшать оценку экспериментально определенной гидратации Даже без таких поправок экспериментальные значения меньше, чем гидратация, вычисленная в предположении об однородности слоя воды, особенно для кагионных ПАВ. Гидратация последних может быть, таким образом, лишь частичной. Если сравнить значение экспериментальной гидратации с расчетами, предполагая некоторые первичные числа гидратации из данных для ионных растворов, то получается разумное соответствие. Поэтому представляется, что гидратация мицелл согласуется с гидратацией полярных групп и противоионов в отсутствие мицеллообразования, и нет необходимости приписывать основной вклад в гидратацию какой-либо льдр-подобной структуре на поверхности [ 33], повышенной вязкости воды на заряженных поверхностях [34] или кооперативному действию зарядов на поверхности мицеллы. [35]
Этот выбор диктуется в основном стремлением сохранить натив-ность очищаемого белка и максимально уменьшить неспецифическую сорбцию других компонентов исходной смеси. Само аффинное связывание вещества с лигандом, как правило, от состава буфера жидкой фазы зависит мало. Интересами сохранения нативности и растворимости белка диктуются выбор рН, наличие соли, а иногда ( например, для белков мебран) введение в буфер добавок органических растворителей или детергентов. Все это определяется известными свойствами данного белка. Неспецифическая сорбция примесей, в частности балластных белков, на матрице и спейсерах происходит за счет тех же самых сил ( притяжения разноименно заряженных групп, водородных связей и гидрофобных взаимодействий), которые обусловливают и биоспецифическое связывание вещества с лигаи-дом. Избирательность и прочность аффинной связи обусловлены кооперативным действием различных сил в области связывания, где они дополняют друг друга. Благодаря такой кооперации имеется возможность ввести в буфер факторы, ослабляющие действие сил какого-либо типа или даже всех их одновременно, но в такой степени, что биоспецифическое аффинное взаимодействие будет ослаблено лишь частично, в то время как неспецифическую сорбцию удастся подавить практически полностью. [36]
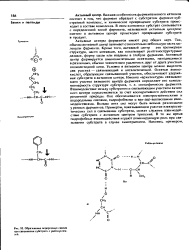 |
Образование водородных связей при связывании субстрата с рнбонуклеа-зой. [37] |
Актианые центры ферментов имеют ряд общих черт. Так, обычно активный центр занимает относительно небольшую часть молекулы фермента. Кроме того, актианый центр это трехмерная структура, часто имеющая, как показывают рентгеноструктурные данные, форму щелн или впадины в глобуле фермента. Активный центр формируется аминокислотными остатками, находящимися в различных, обычно значительно удаленных друг от друга участках полипептидной цепи. Условно в активном центре можно выделить два участка - связывающий и каталитический. Остатки аминокислот, образующие саязывающий участок, обеспечивают удержание субстрата а активном центре. Взаимодействие между субстратом и связывающим участком активного центра осуществляется за счет кооперативного действия сил различной природы. Оно обеспечивается электростатическими и водородными саязями, гидрофобными и ваи-дер-ваальсовыми взаимодействиями. Вклады этих сил могут быть весьма различными у резных фермеитоа. Примером, показывающим участие электростатических сил а связывании субстрата, может служить взаимодействие субстрата с актианым центром трипсине. В то же время гидрофобные взаимодействия играют доминирующую роль при связывании субстрате а случае химотрипсина. [38]
Страницы: 1 2 3