Замедляющее действие
Cтраница 2
Замедляющее действие свинцового сурика в покрытиях, как показали исследования Памфилова и Кипарисова [9], обусловлено главным образом основным характером входящей в его состав окиси свинца. Так, окись свинца при действии воды дает ОН-ионы, которые, находясь вблизи анода, подавляют анодную реакцию вследствие образования гидрата закиси железа в состоянии тесного контакта с металлической поверхностью. [16]
Замедляющее действие цинковой пудры объясняют электрохимической протекторной защитой, потому что цинк по отношению к железу является анодом. Так как в красочном покрытии цинковая пудра не может иметь достаточного непосредственного контакта с металлом, то, очевидно, протекторное действие будет лучше проявляться при водонабухании покрытия. [17]
Замедляющее действие алюминиевой пудры не всегда можно объяснить электрохимической протекторной защитой, так как алюминий по отношению к железу является анодом только в солевых растворах. Очевидно, на защитную способность покрытий с алюминиевой пудрой в значительной мере влияет их малая водонабухаемость и проницаемость в связи с чешуйчатым строением частиц алюминиевой пудры. [18]
Весьма интересное замедляющее действие желатины на процесс сенсибилизации ( рис. 5) нельзя объяснить уменьшением скорости диффузии сульфида. Дополнительные опыты, не приведенные в настоящем сообщении, показывают, что увеличение количества адсорбированной желатины путем предварительного нагревания смеси золя с желатиной не влияет на сенсибилизацию. [19]
Замедляющее действие окиси азота [18] связано, видимо, с тем, что1 она соединяется с органическими радикалами, образуя нитросоединения. Ускоряющее же действие связано с тем, что, будучи скрытым радикалом, окись азота может, хотя и с значительной энергией активации, вступать как радикал в реакцию с исходным веществом и порождать, таким образом, первичные радикалы цепи. Окись азота производит ускоряющее действие и на реакции окисления углеводородов, способствуя зарождению первичных радикалов, видимо, за счет взаимодействия с исходными углеводородами. [20]
Замедляющее действие органических веществ, в противоположность мнению некоторых авторов, обычно проявляется больше при анодном процессе, поэтому потенциал саморастворения в присутствии ингибитора в этих случаях сдвигается в сторону положительных потенциалов. [21]
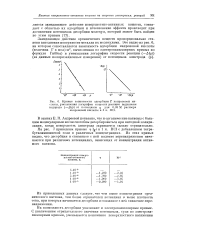 |
Кривые зависимости адсорбции Г капроновой кислоты, уменьшения логарифма скорости реакции выделения водорода ( - AlgO от потенциала р для 0 02 М раствора капроновой кислоты в 2 п. IIC1. [22] |
Замедляющее действие органических веществ пропорционально степени заполнения поверхности металла их молекулами. [23]
Ускоряющее и замедляющее действие катализаторов - металлов переменной валентности, можно проследить на примере окисления многих органических соединений: например, гидроперекись этилбензола, устойчивая при 50 - 80 С в отсутствии катализаторов, распадается с большой скоростью в присутствии, скажем, бис ( а-тиопиколин-анилида) меди. При этом окисление этилбензола в этих условиях идет со значительным торможением, так как продуктами распада гидроперекиси являются молекулярные соединения, а не радикалы. [24]
Учитывая замедляющее действие водорода на процесс общей коррозии конструкционных материалов, некоторые исследователи предположили, что концентрация его примерно от 25 до 50 мл / кг вполне достаточна для предупреждения щелевой коррозии. Однако для проверки этого предположения необходимы были дополнительные испытания. [25]
Хотя замедляющее действие кислот на скорость изомеризации при низкой концентрации кислоты, по-видимому, не сопровождается разложением, было найдено [82], что если через реакционную смесь с концентрацией кислоты, приблизительно равной 0 07 М, пропускать азот, то обнаруживаются небольшие количества окиси азота и акво-комплекса. [26]
Сильнее всего замедляющее действие уротропина проявляется на коррозии железа-армко. [27]
Механизм замедляющего действия в этом случае сводится к контактному выделению металла на корродирующей поверхности и анодному пассивированию свободных ее участков. [28]
Помимо замедляющего действия дифенилнитрозамин обладает еще способностью вновь пластицировать более или менее сильно подвулканизованные смеси. [29]
Оптимум замедляющего действия у ( NH4) 2Mo04 лежит при 10 - 3 М концентрации окислителя. Более высокие концентрации ( NH4) 2Mo04 вызывают увеличение коррозии за счет под-кислсния раствора. Образующаяся при воздействии КМн04 на поверхности образцов бурая пленка периодически разрушается в процессе роста, что приводит к наблюдающемуся усиленному местному растворению железа, сопровождающемуся образованием наростов продуктов коррозии. В 0 01 % - ном NaCl с добавками K2Cr207, Na2W04 и ( NH4) 2Mo04 сдвиг потенциалов железа в положительную сторону сопровождается уменьшением скорости коррозии. В растворах с добавками КМп04 такой закономерности не наблюдается. Однако было установлено, что максимумы коррозии наблюдаются всегда при весьма положительных значениях потенциалов образцов. В 0 01 % - ном NaCI с добавками К2Сг207 сдвиг окислительно-восстановительного потенциала раствора в положительную сторону сопровождается уменьшением скорости коррозии железа. В растворах с добавками Na2W04 наблюдается обрат-пая зависимость: уменьшение скорости коррозии наблюдается при сдвиге окислительно-восстановительного потенциала в отрицательную сторону. Для растворов с добавками ( NH4) 2Mo04 и КМп04 трудно установить какую-либо зависимость между скоростью коррозии железа и окислительно-восстановительным потенциалом раствора. [30]
Страницы: 1 2 3 4