Дифференцирующее действие - ацетон
Cтраница 1
 |
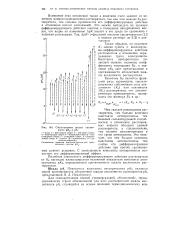
Титрование смеси 0 05 н. пикриновой ( 1 и 0 05 н. трихлоруксусной кислот ( 2 0 1 н. NaOH в 60 % - ном ацетоне. [1] |
Дифференцирующее действие ацетона и его смесей с водой настолько велико, что в этих растворителях удается провести раздельное титрование смеси более двух кислот. [2]
Таким образом, дифференцирующее действие ацетона и, вероятно, других дифференцирующих растворителей на силу кислот является результатом различия в энергии взаимодействия молекул и анионов ( катион у всех кислот один и тот же) кислот разной природы с полярными молекулами растворителей и определяется химическими особенностями последних. [3]
Это можно наблюдать на примере дифференцирующего действия ацетона в отношении дикарбоновых кислот, что видно по изменению Ар / С кислот в его среде по сравнению с водными растворами. Так, АрКа о-фталевой кислоты увеличивается от 2 2 в водном растворе до 5 35 в ацетоновом. [4]
 |
Сопоставление шкалы кислот - растворитель, а следовательно. [5] |
Это можно наблюдать на примере дифференцирующего действия ацетона в отношении дикарбоновых кислот, что видно по изменению Ар / С кислот в его среде по сравнению с водными растворами. [6]
В 1943 году, значительно позже опубликования наших работ по применению дифференцирующего действия ацетона, его свойства были использованы Эйресом и Больфе при кон-дуктометрическом раздельном титровании смеси кислот. Метод состоит в там, что титрование производится в воде - титруются все кислоты; в 40-процентном ацетоне титруются сильные и средние кислоты и в 80-процентном ацетоне титруются только сильные кислоты. [7]
Однако резкое различие в изменении энергии ионов несколько компенсируется изменением энергии недиссоциированных молекул этих же кислот в ацетоне. Отсутствие заметного дифференцирующего действия ацетона на отношение силы уксусной и монохлоруксусной кислоты к силе бензойной кислоты является результатом компенсации этих двух эффектов. [8]
В значительной мере дифференцирующее действие растворителя зависит от сольватирующей способности растворителя. При переходе от одного растворителя к другому энергии сольватации ионов и молекул электролитов изменяются в различной степени. Особенно это изменение становится заметным при переходе от растворителя одной природной группы к растворителю другой природной группы. Так, дифференцирующее действие ацетона и, вероятно, других дифференцирующих растворителей на силу кислот является результатом различия в энергии взаимодействия молекул и анионов кислот различной природы с полярными молекулами растворителя и определяется химическими особенностями растворителей. Однако дифференцирующее действие наиболее отчетливо проявляется при переходе от растворителей одной природной группы к растворителям другой природной группы и также при переходе от электролитов одной химической группы к электролитам другой химической группы. [9]
В значительной мере дифференцирующее действие растворителя зависит от сольватирующей способности растворителя. При переходе от одного растворителя к другому энергии сольватации ионов и молекул электролитов изменяются в различной степени. Особенно это изменение становится заметным при переходе от растворителя одной природной группы к растворителю другой природной группы. Так, дифференцирующее действие ацетона и, вероятно, других дифференцирующих растворителей на силу кислот является результатом различия в энергии взаимодействия молекул и анионов кислот различной природы с полярными молекулами растворителя и определяется химическими особенностями растворителей. Однако дифференцирующее действие наиболее отчетливо проявляется при переходе от растворителей одной природной группы к растворителям другой природной группы и также при переходе от электролитов одной химической группы к электролитам другой химической группы. [10]
Страницы: 1