Каталитическое действие - ион - водород
Cтраница 1
Каталитическое действие ионов водорода на гидролиз комплекс ных анионов является обычным. В первоначальном нейтральном растворе гидролиз должен автокаталитически ускоряться образующимися при гидролизе ионами водорода. [1]
Несмотря на то, что проведенные впоследствии ра-боты [191, 192] подтвердили каталитическое действие иона водорода в реакциях гидролиза и иона гидроксила [193] в реакциях омыления, в ряде случаев нейтральные соли оказывают сильное чисто индивидуальное влияние на скорость исследуемого процесса [ 194, стр. [2]
Следует учитывать, что каталитическое действие ионов металлов совершенно отлично от каталитического действия ионов водорода из-за высокого положительного заряда ионов металлов и вследствие характерной тенденции металлов координировать на своих вакантных d - орбитах электроны субстрата, что приводит к специфическому и избирательному катализу. [3]
Скорость этерификации увеличивается при нагревании и особенно в присутствии минеральных кислот благодаря каталитическому действию ионов водорода. [4]
Если р-нафтол сульфировать серной кислотой даже при комнатной температуре, образующаяся вначале 2 -нафтол - 1-сульфокислота быстро перегруппировывается при каталитическом действии ионов водорода. [5]
Этот механизм согласуется с экспериментально наблюдаемым уравнением скорости v k [ XOj 1 [ Н Р, указывающим на каталитическое действие ионов водорода. Весьма важными являются хлорная кислота и перхлораты. Обычно считается, что НСЮ4 - самая сильная из известных кислот, и это проявляется в неспособности иона СЮ Г давать прочные связи с катионами. В водных растворах ион С1О обычно используется как анион в тех случаях, когда надо избежать комплексообразова-ния. Получить чистую хлорную кислоту довольно трудно. Однако в разбавленных растворах многие реакции окисления ионом С1О - идут очень медленно. [6]
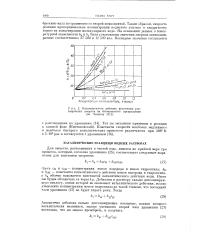 |
Каталитическое действие различных растворенных веществ на бекмановское превращение ( по Чэпмену. [7] |
Здесь CH и CQH - концентрации ионов водорода и ионов гидроксила; & н и / COH - константы каталитического действия ионов водорода и гидроксяла, a kg обычно называется константой каталитического действия воды. Ниже мы будем обозначать ее через k v - Добавляя к раствору сильно диссоциирующую кислоту, анион которой не оказывает каталитического действия, можно уменьшить концентрацию ионов гидроксила до такой степени, что последний член уравнения ( 27) не будет играть роли. [8]
Если р-нафтол сульфировать серной кислотой, то даже при комнатной температуре образующаяся вначале 2-нафтол - 1-сульфокислота быстро перегруппировывается при каталитическом действии ионов водорода. [9]
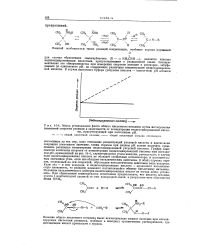 |
Метод установления факта общего кислотного катализа путем исследования изменений скорости реакции в зависимости от концентрации недисеоциированнои кислоты, присутствующей при постоянном рН. [10] |
График зависимости константы скорости от концентрации недиссоциированной кислоты при постоянном рН, приведенный на рис. 14 - 4, характеризуется углом наклона, равным нулю, в случае если недиссоциированная кислота не обладает свойствами катализатора, и положительным значением угла, если она обладает каталитическим действием. В обоих случаях отрезок, отсекаемый на оси скоростей, обусловлен каталитическим действием иона водорода. Если оба - и ион водорода, и недиссоциированная кислота - проявляют каталитическую активность, то реакцию называют подчиняющейся общему кислотному катализу. Механизм каталитического действия недиссоциированных кислот не всегда легко установить. [11]
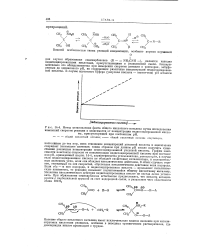 |
Метод установления факта общего кислотного катализа путем исследования изменений скорости реакции в зависимости от концентрации недиссоциированной кислоты, присутствующей при постоянном рН. [12] |
График зависимости константы скорости от концентрации недиссоциированной кислоты при постоянном рН, приведенный на рис. 14 - 4, характеризуется углом наклона, равным нулю, в случае если иедиссоциированная кислота не обладает свойствами катализатора, и положительным значением угла, если она обладает каталитическим действием. В обоих случаях отрезок, отсекаемый на оси скоростей, обусловлен каталитическим действием иона водорода. Если оба - и ион водорода, и недиссоциированная кислота - проявляют каталитическую активность, то реакцию называют подчиняющейся общему кислотному катализу. Механизм каталитического действия недиссоциированных кислот не всегда легко установить. [13]
Изучение гомогенных каталитических реакций в растворах и в газовой фазе указывает на распространенность другого элементарного механизма каталитического воздействия, который играет немалую роль и в гетерогенных системах. При таком механизме окраска катализатора становится несущественной и главную роль играют за ряд и радиус ионов. Существование такого механизма объясняет выдающееся каталитическое действие ионов водорода и гидроксила, солевой эффект и ряд других закономерностей кислотно-щелочного катализа. [14]
 |
Схема изменения концентра - Ф. [15] |
Страницы: 1 2