Использование - пероксид - водород
Cтраница 1
 |
Кинетика фотолитического разложения некоторых фосфорорганических пестицидов. [1] |
Использование пероксида водорода и УФ-облучения для обезвреживания в воде ФОП изучено нами на примере дихлорофоса, хлорофоса, метафоса, карбофоса и фосфамида. [2]
При использовании пероксида водорода, необходимо помнить, что в больших концентрациях он раздражает кожу. Если концентрация раствора превышает 5 %, с ним следует обращаться с осторожностью. При использовании готовых смесей, содержащих пероксид водорода, необходимо соблюдать соответствующую инструкцию. [3]
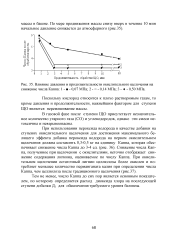 |
Влияние давления и продолжительности окислительного щелочения на снижение числа Каппа. 1-я - 0 07 МПа. 2 - о - 0 14 МПа. 3 - - 0 50 МПа. [4] |
При использовании пероксида водорода в качестве добавки на ступенях окислительного щелочения для достижения максимального белящего эффекта добавка пероксида водорода на первом окислительном щелочения должна составлять 0 3 - 0 5 кг на единицу Каппа, которая обеспечивает снижение числа Каппа до 3 - 4 ед. Снижение числа Каппа, полученное при щелочении с окислителями, неточно отображает снижение содержания лигнина, оцениваемое по числу Каппа. [5]
 |
Технологическая схема интегрированного способа получения. [6] |
Этот способ, основанный на использовании пероксида водорода для восстановления хлората до диоксида хлора при атмосферном давлении, был запатентован в 1984 году. [7]
Разработаны различные методики окисления органических веществ с использованием пероксида водорода. В большинстве из них применяют смесь пероксида водорода с каким-либо другим реагентом. [8]
Фирмой Akzo Nobel предложена технология отбелки целлюлозы с использованием пероксида водорода, которая получила название ЛИГ-НОКС. Данная технология предполагает схему обработки целлюлозы в следующей последовательности: КЩО-Q-II. Обработка ЭДТА проводится в течение 30 мин. Регулирование рН до 4 5 производится серной кислотой. Расход ЭДТА составляет 0 2 % к массе целлюлозы. [9]
Патент США, № 4059678, 1977 г. Рассматривается использование пероксида водорода при кислотной обработке металлов, например, при травлении, и в основном, стабилизация пероксида в таких растворах, где присутствуют примеси железа. Водный пероксид водорода в чистом виде стабилен длительное время. Однако присутствие в растворе ионов тяжелых металлов приводит к более или менее быстрому его разложению. Большинство работ по стабилизации пероксида в присутствии ионов тяжелых металлов касаются стабильности его при хранении в концентрированном или разбавленном виде, часто с водой, содержащей такие тяжелые металлы. [10]
Наблюдаемая хемилюминесценция является дополнительным аргументом при обсуждении механизма окислительной деструкции хитозана. При использовании пероксида водорода свечение, предположительно, возникает из-за диспропорционирования перекисных радикалов, которые образуются в процессе окислительной деструкции хитозана. На основании полученных данных предложен механизм окислительной деструкции хитозана под действием пероксида водорода. [11]
Разнообразие разработанных методов окисления алкенов ( в монографии Ларока [191] перечислено более 80 различных окислительных систем) делает возможным проведение селективного окисления олефинового фрагмента при наличии в структуре самых различных функциональных групп. Так, использование пероксида водорода в щелочных условиях позволяет селективно эпоксидировать двойную связь в ос р-непредельных карбонильных соединениях. [12]
Разнообразие разработанных методов окисления алкенов ( в монографии Ларока [191] перечислено более 80 различных окислительных систем) делает возможным проведение селективного окисления олефинового фрагмента при наличии в структуре самых различных функциональных групп. Так, использование пероксида водорода в щелочных условиях позволяет селективно эпоксидировать двойную связь в х р-непредельных карбонильных соединениях. [13]
Разнообразие разработанных методов окисления алкенов ( в монографии Ларока [191] перечислено более 80 различных окислительных систем) делает возможным проведение селективного окисления олефинового фрагмента при наличии в структуре самых различных функциональных групп. Так, использование пероксида водорода в щелочных условиях позволяет селективно эпоксидировать двойную связь в а ( 3-непредельных карбонильных соединениях. [14]
Оксазиридины были впервые выделены в 1952 г., хотя в более старой литературе такое строение иногда приписывалось нитронам. Другим удобным методом является использование пероксида водорода в присутствии нитрила ( схема 1); реакцию можно проводить в водном или водно-спиртовом растворе. [15]
Страницы: 1 2