N-окись
Cтраница 1
N-Окись была превращена авторами в бен-зилоксипроизводное; последнее о щелочью образует бензальде-гид. [1]
N-Окись акридина представляет собой желтое твердое вещество; в спиртовом растворе она флуоресцирует зеленым цветом. N-Окись акридина является слабым основанием; ее хлоргидрат можно получить в среде бензола. [2]
Неароматические N-окиси этим способом не восстанавливаются. [3]
N-Окись акридина представляет собой желтое твердое вещество; в спиртовом растворе она флуоресцирует зеленым цветом. N-Окись акридина является слабым основанием; ее хлоргидрат можно получить в среде бензола. [4]
N-окисей; кол-во последних может доходить до 90 % от общей суммы алкалоидов. [5]
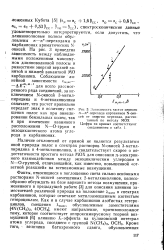 |
Зависимость частот первого я-л - перехода карбанинов N-окисей от энергии перехода, рассчитанной по методу МОХ Цифры на кривых соответствуют соединениям в 1. [6] |
N-окисей 3-метил-пиридина и 4-метилхинолина означает, что расчет правильно передает знак и величину смещения полос как при аннели-ровании бензольных колец, так и при изменении взаимного расположения N - О-групп и экзоциклического атома углерода в карбанионах. [7]
Из N-окиси бензонитрила получены З - фенил-5 - этинилизокса-зол и 3 3 -дифенил - 5 5 -биизоксазол, а из N-окиси лг-хлорбензо-нитрила - 3 - л - хлорфенил-5 - этинилизоксазол и 3 3 -ди - ( ж-хлор-фенил) - 5 5 -биизоксазол. Выделенные с небольшими выходами продукты представляют собой труднорастворимые кристаллические вещества. [8]
Эти N-окиси легко восстанавливаются в соответствующие пиридоксин и пиридоксаль. [9]
Если N-окись шрадана существует, то она должна быть даже менее стойкой, чем Оксиметилшрадан и, следовательно, в схеме, предложенной Хитом и др., также нет необходимости привлекать ферментативный гидролиз для объяснения ее разрушения. [10]
Получены ранее неизвестные N-окиси 5 5-дизамещенных акриданов и исследованы их спектры ЭПР. [11]
Нитрование N-окиси З - метил-4 - фенилциннолина приводит к образованию четырех мононитропроизводных. [12]
Деградация N-окисей ос-кодеинметина CXIXa и р-кодеинме-тина СХХа и N-окисей их метиловых эфиров CXIX6 и СХХб приводит, соответственно, к винильным соединениям CXXIa, CXXIIa, CXXI6 и СХХИб. [13]
Смесь N-окиси 2-пиколина, серы и анилина в этих условиях образует анилид тиопиколино-вой кислоты ( - 40 %), 2 - ( пир Идил-2) - бензотиазол ( - 30 %) [ ср. [14]
Нитрование N-окиси З - метил-4 - фенилциннолина приводит к образованию четырех мононитропроизводных. [15]
Страницы: 1 2 3 4