Дихинона
Cтраница 1
Дихиноны получаются также из соответствующих полиоксиантра-хинонов при окислении перекисью свинца в растворе ледяной уксусной кислоты или в индиферентном растворителе, например бензоле. [1]
 |
Спектр поглощения. [2] |
Раствор этого дихинона в концентрированной серной кислоте окрашен в коричневато-красный цвет. [3]
Наряду с реакциями 1 4-присоединения дихиноны вступают в реакции 1 2 - и 1 6-присоединения. Бром в растворе бромистого калия присоединяется к 1 4 9 10-антрадихинону по связи 2 3, давая дибро-мид XXII, превращающийся при действии йодистого водорода в хинизарин, при обработке бисульфитом - в 2-бромхинизарин и в уксусном ангидриде в присутствии серной кислоты - в диацетат 2 3-дибромхинизарина. [4]
Наряду с реакциями 1 4-присоединения дихиноны вступают в реакции 1 2-и 1 6-присоединения. Бром в растворе бромистого калия присоединяется к 1 4 9 10-антрадихинону по связи 2 3, давая дибро-мид XXII, превращающийся при действии йодистого водорода в хинизарин, при обработке бисульфитом - в 2-бромхинизарин и в уксусном ангидриде в присутствии серной кислоты - в диацетат 2 3-дибромхинизарина. [5]
Так как при окислении исходного ангулярного нафтантрацена всегда образуются одновременно моно - и дихиноны, причем первый при дальнейшем действии окислителя не превращается во второй, а сгорает, переходя через промежуточное, способное давать куб соединение, то авторы сделали предположение, что их исходное вещество состоит из двух изомерных углеводородов. Последние, вероятно, образуют между собой молекулярное соединение, так как участвуют в смеси в равных количествах и не могут быть разделены кристаллизацией. Дальнейшее исследование показало, что монохинон, вопреки принятому ранее, не имеет углеродного скелета, соответствующего ангулярной формуле III, но построен линейно. Это следует из того, что при сплавлении с КОН диметильный дериват этого монохинона дал нафтойные кислоты, а не смесь метилантраценкарбоновой и толуиловой, как это нужно было бы ожидать, если бы его строение было ангулярным. [6]
Кроме дифенохинона, в дифениловом ряду могут существовать и другие хиноны, а также дихиноны. [7]
Дифталил 370, 398 Дифталиловая кислота 229, 230 Дихиноилтетроксим 258 Дихинолилкетон 67 е - Дихинолилметан 67 Дихиноны 103, 116 ел. [8]
Проведенное сопоставление модельных соединений приводит к заключению, что тенденция к замыканию водородной связи в про-тонированной форме производных антрахинона должна убывать в последовательности: антрахинонпиридины антрахинонпирази-ны дихиноны - антрахинондиазолы. Для антрахинондиазолов, в отличие от остальных рассмотренных хигюпов, возникновение внутримолекулярной водородной связи не может играть существенной роли. [9]
Проведенное сопоставление модельных соединений приводит к заключению, что тенденция к замыканию водородной связи в про-гонированной форме производных антрахинона должна убывать в последовательности: антрахинонпиридины антрахинонпирази-ны дихиноны антрахинондиазолы. Для антрахинондиазолов, в отличие от остальных рассмотренных хинонов, возникновение внутримолекулярной водородной связи не может играть существенной роли. [10]
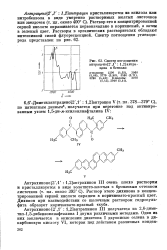
При окислении 3 4 - 8 9-дибензтетрафена III избытком хромовой кислоты в ледяной уксусной кислоте получается дихинон V. Раствор этого дихинона в серной кислоте окрашен в коричневый цвет. [11]
Его раствор в концентрированной серной кислоте окрашен в коричневый цвет. При обработке щелочным раствором гидросульфита натрия дихинон V образует фиолетовый куб, который быстро изменяет окраску на коричневую. В присутствии кислорода воздуха из этого раствора выпадает зеленый осадок. [12]
Конденсация фенантрена с избытком фталевого ангидрида в тет-рахлорэтане при 95 С в присутствии хлористого алюминия дает смесь дикарбоновых кислот, из которой кристаллизацией выделяют индивидуальную дикарбоновую кислоту, имеющую, вероятно, структуру I. Циклизация этой кислоты под действием серной кислоты приводит к дихинону II, из которого гептафен III получается восстановлением цинковой пылью в пиридине и уксусной кислоте. [13]
Фриделя-Крафтса с фенантреном должна приводить к смеси изомеров, в действительности получается только одна дикарбоновая кислота IV - производное терефталевой кислоты или изомерной ей изофталевой кислоты. Циклизация этой кислоты под действием хлористого бен-зоила в присутствии следов серной кислоты приводит к дихинону V, восстановление которого цинке / вой пылью в пиридине и уксусной кислоте дает 6 13-дигидротетрабензпентацен II, оказавшийся идентичным углеводороду, полученному предыдущим методом. Дегидрирование дигидропроизводного II в тетрабензпентацен III осуществлено путем возгонки над палладием на угле при 370 С. [14]
Смесь кислот, полученных из пирена действием избытка фтале-вого ангидрида и хлористого алюминия в тетрахлорэтане, содержит главным образом кислоту I. Циклизация этой кислоты при обработке бензоилхлоридом в кипящем нитробензоле в присутствии следов серной кислоты приводит к дихинону II, который может быть восстановлен в углеводород III цинковой пылью и уксусной кислотой в пиридине или сплавлением с цинковой пылью. [15]
Страницы: 1 2