Дихлорид - цирконий
Cтраница 1
Дихлорид циркония представляет собой блестящее аморфное вещество черного цвета с плотностью 3 6 г / см3; оно плохо растворяется в спирте, эфире, бензоле, растворяется при нагревании в концентрированных кислотах с выделением водорода. [1]
Дихлорид циркония в свою очередь при нагревании в течение нескольких часов при 650 С разлагается частично на тетрахлорид и металлический цирконий. [2]
Три - и дихлорид циркония являются более устойчивыми соединениями, чем три-и дихлорид гафния. [3]
Три - и дихлориды циркония устойчивее, чем три - и дихлориды гафния. [4]
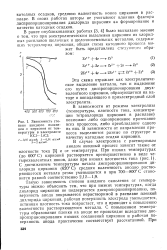 |
Зависимость сте. [5] |
В своих работах авторы не учитывают влияния фактора диспропорционирования дихлорида циркония аа формирование и качество катодных осадков. [6]
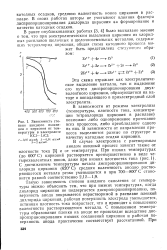 |
Зависимость сте. [7] |
Такую зависимость степени анодного окисления от температуры можно объяснить тем, что при низких температурах, когда дихлорид циркония не подвергается диспропорционированию, поверхность анода покрывается нерастворимой в расплаве пленкой дихлорида циркония, рабочая поверхность электрода уменьшается, истинная плотность тока возрастает, что и приводит к повышению валентности растворяющегося металла. С повышением температуры образования пленки на аноде не происходит вследствие диспропорционирования низших соединений циркония и рабочая поверхность анода практически соответствует рассчитанной. [8]
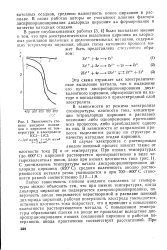 |
Зависимость сте. [9] |
Такую зависимость степени анодного окисления от температуры можно объяснить тем, что при низких температурах, когда дихлорид циркония не подвергается диспропорционированию, поверхность анода покрывается нерастворимой в расплаве пленкой дихлорида циркония, рабочая поверхность электрода уменьшается, истинная плотность тока возрастает, что и приводит к повышению валентности растворяющегося металла. С повышением температуры образования пленки на аноде не происходит вследствие диспропорционирования низших соединений циркония и рабочая поверхность анода практически соответствует рассчитанной. [10]
Известно, что на процесс электрокристаллизации поливалентных металлов из расплавленных хлоридов влияет концентрация ионов этих металлов различной валентности и их соотношение в электролите. Во время электролиза в прикатодном слое вследствие электрохимического восстановления тетрахлорида циркония образуется дихлорид циркония, который в зависимости от условий электролиза или электрохимически восстанавливается до металла, или распадается по реакции диспро-порционирования. [11]
 |
Количественное соотношение анодного и катодного процессов. [12] |
Следовательно, при низких анодных плотностях тока основная доля растворившегося металла сосредотачивается в электролите в виде находящейся в динамическом равновесии смеси мелкодисперсного металла ди - и тетрахлорида циркония. Такое распределение продуктов анодного растворения циркония еще раз говорит о том, что дихлорид циркония практически нерастворим в расплавах хлоридов щелочных металлов и существует в них лишь в контакте с металлом. Нарушение равновесия между анодным и катодным процессами, увеличивающееся с уменьшением анодной плотности тока, свидетельствует о том, что образующийся на аноде двухвалентный цирконий непосредственно не участвует в катодном процессе. Следовательно, анодная плотность тока в случае-циркония, дихлорид которого практически нерастворим в изучаемых расплавах, не может влиять на процесс электрорафинирования так, как это имеет место в случае титана, низшие хлориды которого растворимы в хлоридных расплавах. [13]
Процесс ведется при атмосферном давлении. Тетрахлорид циркония возгоняется при 335 С и вводится в абсорбер с нагретым до 390 - 400 С дихлоридом циркония. Твердый трихлорид поступает в аппарат разложения, работающий при температуре 420 - 450 С. [14]
Возможна очистка ZrCl4 от HfCl4, основанная на различной степени восстановления этих хлоридов [ 37; 50, с. Смесь хлоридов циркония и гафния ( 98 5 % ZrCl4, 1 5 % HfCl4) пропускают через нагретый металлический цирконий или дихлорид циркония при 400 С. Твердый остаток, содержащий ZrCla, ZrCl2 и непрореагировавший Zr нагревают до 450 С в вакууме. В результате диспропорционирования низших хлоридов по реакциям (12.1) и (12.2) выделяется очищенный ZrCl4 с содержанием около 0 05 % HfCl4, a ZrCl2 и Zr вновь направляют для восстановления технического продукта. [15]
Страницы: 1 2