Использование - стеклянный электрод
Cтраница 3
В случае амминов меди удовлетворительные и воспроизводимые результаты были получены при измерении давления паров аммиака и светопоглощения, а также при использовании медного электрода. Однако применение этих методов было связано с довольно длительной и трудоемкой работой. Поэтому использование стеклянного электрода в качестве универсального прибора для быстрого и удовлетворительного исследования процесса образования амминов в растворе оказалось исключительно прогрессивным. Рассмотрим этот вопрос более подробно. [31]
Далеко не во всех случаях потенциометрического титрования возможно применение дифференциального титрования. Часто, даже когда кривая титрования содержит ясно различимый скачок потенциала, но недостаточно резкий, электронный сигнализатор, несмотря на специальные меры по повышению его помехоустойчивости, оказывается не в состоянии четко отличать сигнал от помех. Особенно часто это имеет место при использовании стеклянных электродов, а также при неводном титровании. [32]
Старые методы определения концентрации ионов водорода с использованием водородного и хингидронного электродов непригодны для изучения амминов, так как эти электроды обычно отравляются в аммиачном растворе солей металлов. Колориметрический метод, если он вообще применим, недостаточно точен. Стеклянный электрод в этих случаях имеет преимущество: он позволяет измерять рН с большой точностью в любом растворе. Единственное ограничение при использовании стеклянного электрода заключается в том, что раствор не должен быть сильно щелочным ( рН 10), иначе он будет разъедать стекло. [33]
Синха [25] разделял катионообменной мембраной два раствора соляной кислоты, а затем оттитровывал один из растворов гидроокисью натрия, периодически измеряя мембранный потенциал во время титрования. Уравнение ( 96) в этом случае неприменимо, потому что в титруемом растворе находятся два вида катиона вплоть до конечной точки титрования. Несмотря на это, точка эквивалентности отмечается скачком на кривой титрования. Этот способ титрования не рекомендуется из-за большей: трудоемкости и меньшей точности, чем при использовании стеклянного электрода или индикатора. [34]
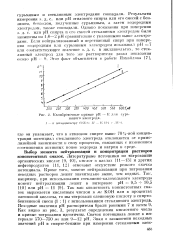 |
Калибровочные кривые рН - Е для сурьмяного электрода. [35] |
Литературные источники по титрованию органических кислот [ 9, 10J, кислот в маслах [11 -13] и других нефтепродуктов Щ, 12 J отмечают отсутствие резкого скачка потенциала. Кроме того, момент нейтрализации при титровании неводных растворов лежит значительно выше, чем водных. Так как кислотность консистентных смазок выражается кислотным числом в мг КОН или в процентах олеиновой кислоты, то мы титровали олеиновую кислоту в снирто-бензиновой смеси ( 1: 1) с использованием стеклянного электрода. Как видно из рис. 3, результат определения кислотного числа и кривые титрования идентичны. [36]
Установление потенциалов происходило быстро в растворах хлоридов марганца ( II) и железа ( II), хотя добавление тетрасульфоната индиго в некоторой степени, по-видимому, замедляло установление потенциалов в последнем случае. В растворах кобальта ( II) и особенно никеля, потенциалы устанавливались значительно медленнее. В то время как при титровании кобальта ( II) постоянный потенциал устанавливался в течение 5 - 15 мин. В связи с медленным установлением потенциалов и соответствующей неточностью определения концентрации водородных ионов были дополнительно произведены титрования растворов кобальта ( II) и никеля с использованием стеклянного электрода. [37]
Страницы: 1 2 3