Использование - ртутный электрод
Cтраница 2
Металлическая ртуть - яд, и поэтому при работе с ней необходимо строго соблюдать правила техники безопасности. Особенно ядовиты ее пары, поэтому все работы по полярографии с использованием ртутных электродов должны проводиться в помещении со специально оборудованным вентиляционным устройством. Штатив с электролитической ячейкой следует установить в специальную кювету и поместить в вытяжной шкаф. Столы и пол в помещении, где проводятся работы с ртутью, должны быть покрыты линолеумом или другим подобным материалом с герметично заделанными швами. [16]
При работе на твердых электродах отсутствуют осцилляции, что увеличивает точность и быстроту отсчетов. Большой недостаток твердых электродов в том, что при работе с ними воспроизводимость определений хуже, чем при использовании ртутных электродов, так как поверхность электрода трудно сохранить всегда в неизменном состоянии. Особенно это относится к амальгамированным электродам. [17]
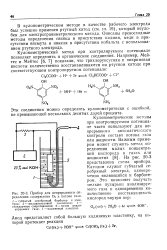 |
Прибор для непрерывного определения содержания О2 в потоке газа. [18] |
В кулонометрическом методе в качестве рабочего электрода был успешно применен ртутный катод ( см. гл. Описаны превосходные методы определения свинца в присутствии кадмия, меди в присутствии висмута и никеля в присутствии кобальта с использованием ртутного электрода. [19]
Методом пленочной полярографии могут быть определены некоторые анионы ( С1 -, Br -, S2 -, Мо042 -, W042 -, Cr042 -, V03-и др.), образующие с материалом электрода малорастворимые соединения. Предложены методы определения СГ -, J -, S2 - в уране [49] и в солях высокой чистоты [50] с использованием ртутного электрода. Шейн и С. П. Перон [52] и В. М. Гороховский [53] показали, что применение Ag-электрода для определения галогенидов в водных и спиртово-водных растворах дает возможность повысить чувствительность определения, например, J - до 4 - 10 - 8 молъ / л, что связано с меньшей пассивацией этого электрода, чем Hg-электрода. [20]
 |
Значения рН в процессе осаждения гидроксидов металлов. [21] |
Сточные воды, загрязненные ртутью и ее соединениями, образуются при производстве хлора и едкого натра, в других процессах электролиза с использованием ртутных электродов, на ртутных заводах, в некоторых гальванических производствах, при изготовлении красителей, углеводородов, на предприятиях, использующих ртуть как катализатор. [22]
 |
Некоторые типы стационарных ртутных электродов. [23] |
Так как восстановление ионов водорода на ртути связано со значительно более высоким перенапряжением, чем на благородных металлах, особенно широкое применение ртутные электроды нашли в вольтамперометрии. Замена ртути на благородные металлы связана с введением в измерительную систему электродов с шероховатой поверхностью, что приводит к менее воспроизводимым вольт-амперным кривым по сравнению с кривыми, полученными с использованием ртутных электродов. Даже если поверхность твердого электрода отполировать, все равно она далека от идеальной, гладкой поверхности ртути. [24]
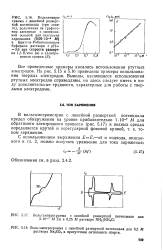
На рис. 5.15 и 5.16 приведены примеры использования твердых электродов. Выводы, касающиеся использования ртутных электродов справедливы, но здесь следует иметь в виду дополнительные трудности, характерные для работы с твердыми электродами. [26]
В полярографии изучают кривые ток - потенциал, являющиеся результатом процесса переноса электрона, который происходит на поверхности ртутного капающего электрода, площадь которого составляет всего несколько квадратных миллиметров. В своей Нобелевской лекции Гейровский рассмотрел некоторые из достоинств полярографии, а именно: возможность анализировать растворы, разбавленные до 10 - 5 М, при использовании ртутных электродов анализировать пробы, объем которых составляет до 0 05 мл, и возможность определить почти каждый элемент, находящийся в той или другой форме, а также многие сотни органических соединений. [27]
Из уравнения (7.34) следует, что в этом случае в отличие от ранее обсужденных случаев потенциал полуволны является функцией концентрации деполяризатора в объеме раствора. При десятикратном увеличении концентрации деполяризатора потенциал полуволны смещается на 2 303 RTInF в направлении положительных потенциалов. Уравнение (7.32) трудно проверить экспериментально. С одной стороны, при использовании ртутного электрода трудно найти металл, практически нерастворимый в ртути, ионы которого обратимо восстанавливаются на ртутном электроде. С другой стороны, если для проверки уравнения используют твердые электроды, например платиновые, то в начальный период, пока восстанавливаемый металл не полностью покрывает электрод, активность металла меняется. Это противоречит уравнению (7.32), из которого было выведено уравнение волны. [28]
При этом на полярограмме при E Ei / 2 наблюдается максимум, высота которого пропорциональна концентрации. Ограничения метода полярографического анализа связаны с использованием ртутного электрода. [29]
Страницы: 1 2 3