Дихромат
Cтраница 2
 |
Ус. юаня окисления органических псщсстг хрс-мотй кислотой и хромитами. [16] |
Окисление дихроматом может быть использовано при определении и других элементов. Как уже отмечено выше, хлориды и бромиды окисляются до свободных элементов, которые можно выделить из раствора нагреванием. [17]
Между дихроматом связного графа и множеством его остовов существует тесная взаимосвязь. [18]
В дихромате цезия калия содержится меньше. [19]
С раствором дихромата прореагировало ( 35 0 - 15 0) х X 0 045 - 10 - 3 г-экв соли железа ( П), что соответствует содержанию в 9 672 г стали 10 - 0 900 - 10 - 3 - 52 / 30 156 г хрома. Следовательно, процентное содержание хрома ( по массе) составляет ( 0, 156: 9 672) 100 1 61 % хрома. [20]
Вместо раствора дихромата для установления титра раствора тиосульфата можно взять раствор перманганата калия, применявшийся при перман-ганатометрическом анализе. [21]
Титр раствора дихромата очень устойчив, и раствор можно хранить длительное время. [22]
После добавления дихромата возникает красно-коричневое окрашивание, при разбавлении водой и перемешивании раствор желтеет, а после подщелачивания аммиаком происходит незначительное потемнение раствора. [23]
Из восстанавливаемости дихромата в силу соотношений (IX.6.1), (IX.2.1) и (IX.4.1) вытекает восстанавливаемость дихроматического, хроматического и потокового многочленов. В частности, восстанавливаемой характеристикой графа является его хроматическое число, а восстанавливаемым свойством - существование или отсутствие в графе 5-потока. [24]
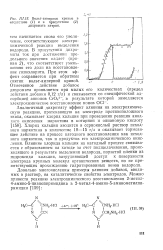 |
Вольт-амперные кривые в. [25] |
В присутствии дихромата ток при достижении предельного значения падает ( кривая 2), что соответствует уменьшению его доли на восстановление гипохлорита. При этом эффект сохраняется при обратном снятии вольт-амперной кривой. [26]
При титровании дихроматом применяют окислительно-восстановительные индикаторы: дифениламин или фени-лантраниловую кислоту, меняющие свою окраску при незначительном избытке дихромата в титруемом растворе. Эти индикаторы меняют окраску в результате перехода восстановленной формы в окисленную, их называют окислительно-восстановительными индикаторами. [27]
Поэтому титруют дихроматом в кислой среде. [28]
Переход хромата в дихромат и обратно. [29]
Если к раствору дихромата прибавлять щелочь, то гидроксильные ионы будут связывать находящиеся в растворе ионы водорода, равновесие смещается влево и в результате дихромат превращается в хромат. [30]
Страницы: 1 2 3 4