Диэтилсульфоксид
Cтраница 1
Диэтилсульфоксид в лабораторных условиях можно получить с выходом 70 5 % электролитическим окислением диэтил-сульфида в смеси уксусной и соляной кислот в приборе с анодом з платиновой сетки. [1]
 |
Значения частот ( в см - ] валентных колебаний связей Pt - С1в комплексах цас - и транс - [ РЩДМСО С12 ]. [2] |
Сравнение положения диэтилсульфида и диэтилсульфоксида показывает, что сульфоксиды в большей степени способствуют закреплению хлора в транс-положении. Наличие кислорода при атоме серы должно повышать эффективный заряд атома сульфоксидной серы по сравнению с сульфидной. Методом рентгеновской эмиссионной спектроскопии действительно показано, что эффективный положительный заряд на атоме серы в сульфоксиде выше, чем в сульфиде. Такой же вывод был сделан на основании кислотных свойств аналогичных сульфидных и сульфоксидных соединений. Более высокий положительный эффективный заряд может являться причиной несколько больших я-акцепторных свойств сульфоксидов по сравнению с соответствующими сульфидами. Однако эффективный заряд не единственная причина, которая может сказываться на л-акцепторных свойствах лигандов. [3]
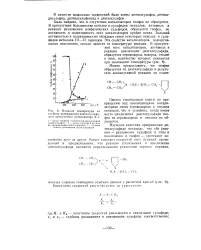 |
Влияние температуры на глубину превращения диэтилсульфида в присутствии катализатора К-1. [4] |
В качестве модельных соединений были взяты диэтилсульфид, диэтил-дисульфид, диэтилсульфоксид и диэтилсульфон. [5]
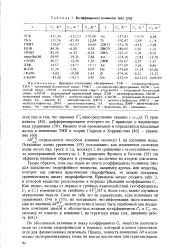 |
Коэффициенты полинома ( 46. [6] |
Приняты следующие обозначения: ТГФ - тетрагидрофуран, ТБА - третичный бутиловый спирт, ГМФТ - гексаметилфосфортриамид, EtOH - этиловый спирт, / РгОН - изопропиловый спирт, втор - ВиОН - вторичный бутиловый спирт, - РгОН - нормальный пропиловый спирт, ДЭФ - диэтилформамид, МеОН - метиловый спирт, / ВиОН - изобутиловый спирт, и - BuOH - нормальный бутиловый спирт, Ац - ацетон, ЭГ - этиленгликоль, ДЭСО - диэтилсульфоксид, ДМСО - ди-метилсульфоксид, ДМА - диметилацетамид, АА - ацетамид, ДМФ - диметилформ-амид, Ан - ацетонитрил, Пн - пропионитрил, Ф - формамид, Мч - мочевина. [7]
Если функция представлена двухвалентной группой или атомом ( например, - О - или СО), то присоединенные к ней две различные группы записываются в алфавитном порядке. Примерами могут служить названия: бензилфениловый эфир, диэтиловый эфир, бензилнафтил-1 - сульфид и диэтилсульфоксид. [8]
Насколько известно автору, до настоящего времени еще не получен ферментный препарат, вызывающий распад сульфоксида до меркаптана. Описаны только два случая биологического расщепления сульфоксидов - восстановление до соответствующих сульфидов диметил - и диэтилсульфоксидов культурами Scopulariopsis brevicaulis, выращенными на хлебной среде. [9]
В заключение следует остановиться на некоторых аналитических методах определения сульфидов. Окисление диэтилсульфида персульфатом калия в буферном растворе кислого одно-замещенного фосфата калия протекает ступенчато, сначала до диэтилсульфоксида, а затем - до диэтилсульфона. [10]
СУЛЬФОКСИДЫ ( сульфоокиси, окиси сульфидов) - органич. Диме-тил - и диэтилсульфоксиды - вязкие жидкости, затвердевающие при охлаждении. [11]
Более медленную циклизацию метилэтил -, этилпропил - и дипропилсульфидов можно объяснить локировкой циклизующих центров катализатора легко крекирующимися продуктами распада указанных соединений. Меньшая скорость образования тиофена из диэтилсульфоксида или сульфона по сравнению с диэтилсульфидом, возможно, обусловлена протеканием конкурирующих реакций взаимодействия SO и SO2 групп с водородом, а также некоторым изменением состава катализатора в условиях этих реакций. Энергии активации циклизации почти всех изученных соединений близки ( табл. 61), что позволяет предположить одинаковый механизм превращения этих соединений в тиофены. [12]
Для установления детального механизма реакции образования тиофенов из тиоэфиров, в частности для проверки высказанного предположения о протекании реакции циклизации через стадию разрыва С-S связей в молекуле алифатического тиоэфира, изучено [484, 495, 532, 561] превращение тиоэфиров разного строения в интервале температур 300 - 600 С, т0 5 - 5 с в присутствии сульфидных катализаторов. В табл. 59 приведен перечень использованных тиоэфиров, а также для примера состав тиофенов, содержащихся в некоторых катализатах после опыта. Эти данные показывают, что из тиоэфиров получаются тиофены иного строения, чем можно было бы ожидать от внутримолекулярной дегидроциклизации тиоэфира. Состав продуктов находится в соответствии с предположением о протекании реакции цик-лиз ации тиоэфиров в тиофены через стадию распада по С-S связям, дегидрирования углеводородного фрагмента и его конденсации с атомами серы. Действительно, если верна схема 10, тиофен должен образовываться не только из диэтилсульфида, но и метилэтилсульфида, внутримолекулярная циклизация которого невозможна, а также диэтилдисулъ-фида, диэтилсульфоксида. [13]
Страницы: 1