Диэтилциклогексан
Cтраница 1
Диэтилциклогексан образует в основном тетраметилщшло-гзксан и бутаны. [1]
Диэтилциклогексан образует главным образом тетраметил-циклогексан, но в случае отщепления этильных групп эти последние дают бутан. [2]
Диэтилциклогексан - бесцветная жидкость с эмпирической формулой С ] 0Н2о и мол. [3]
Диэтилциклогексан прост и дешев, его производство организуется на базе стирола, при котором в качестве побочного продукта получается этилбен-зол. После гидрирования его переводят в Диэтилциклогексан. [4]
Фракция СюН2о представляла собой смесь - бутил - и диэтилциклогексана. Среди углеводородов СнН28 был найден к-октилциклогексан. [5]
В этом случае результаты расчетов совпадают с экспериментальными данными для равновесий 1 3-диизопропилциклогексанов не так хорошо, как для диэтилциклогексанов. По-видимому, это связано с тем, что при температуре эксперимента заметные количества диизопропил-циклогексанов существуют в гибкой форме. [6]
Цель настоящей работы - рассмотреть влияние эффективной добавки, ингибирующей полимеризацию и приводящей к образованию этилциклогексана ( в качестве основного продукта), а также небольших количеств бутил - и диэтилциклогексана. [7]
Дихлор-1 - нитропропан 341 1 1 - Дихлор-1 - нитроэтан 341 Дихлорпентаны 188, 190 2 3 - Дихлор-к-пентан 180 1 1 - Дихлорпропан 164, 176 1 2 - Дихлорпропан 164, 176, 358, 590 1 3 - Дихлорпропан 136, 163, 176, 215 2 2 - Дихлорпропан 164, 176 1 4 - Дихлорциклогексан 388 Дихлорэтан 54, 174, 546, 591 Дихлорэтилен 155 Дициклогексил 373 1 1 - Дициклогексилгекса декан 237 Дициклогексилмстан 373 Диэтилкарбинол 222 Диэтилциклогексан 520 Додекан 58, 199, 230, 552 ел. [8]
Диэтилциклогексан прост и дешев, его производство организуется на базе стирола, при котором в качестве побочного продукта получается этилбен-зол. После гидрирования его переводят в Диэтилциклогексан. [9]
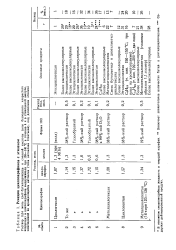 |
Реакция циклопарафинов с этиленом. [10] |
Включает значительное количество бутил - и диэтилциклогексана. [11]
Оптически активный этиловый эфир цинхолойпона ( а), полученный из дигидроцинхонина, был путем последовательного восстановления превращен в 3 4-диэтилпиперидин. Это соединение при расщеплении с помощью РВг5 ( по Брауну) дало дибромид, который конденсацией с натриймалоновым эфиром и затем декарбоксилированием образующейся дикарбоновой кислоты был превращен в диэтилциклогексанкар-боновую кислоту. Полученный диэтилциклогексан, в противоположность всем промежуточным продуктам, оказался оптически неактивным. [12]
Гомологи циклогексана с более длинными цепями ( С Н5, С3Н7 и CjHjj) претерпевали превращения более сложного типа: за счет отщепления боковых групп здесь частью происходило образование низших парафинов и циклогсксепа, который превращался под влиянием хлористого алюминия в высокомолекулярные продукты полимеризации; частью же наблюдалось образование метилированных гомологов циклогексана, очевидно, за счет отщепления мстплышх групп от исходных углеводородов с последующим присоединением отих групп в новом положении. Так, например, диэтилциклогексан превращается в этих условиях главным образом в тетраметилциклогексан, бутан и продукты уплотнения. [13]
Гомологи циклогексана с более длинными цепями ( С2Н5, С3Н7 и С5На1) претерпевали превращения более сложного типа: за счет отщепления боковых групп здесь частью происходило образование низших парафинов и циклогексена, который превращался под влиянием хлористого алюминия в высокомолекулярные продукты полимеризации; частью же наблюдалось образование метилированных гомологов циклогексана, очевидно, за счет отщепления метильных групп от исходных углеводородов с последующим присоединением этих групп в новом положении. Так, например, диэтилциклогексан превращается в этих условиях главным образом в тетраметилциклогсксап, бутан и продукты уплотнения. [14]
Страницы: 1