Исследование - кинетика - превращение
Cтраница 1
Исследование кинетики превращения С-центров в Л - центры под действием температуры показало, что она хорошо описывается феноменологическим уравнением Авраами, которое широко используется для описания процессов распада твердых пересыщенных растворов. Величина параметра процесса п свидетельствует о сферической форме Л - центров, или о прямоугольной и округлой формах пластин. Обращают на себя внимание более высокое значение энергии активации и низкая скорость процесса превращения С-центров в Л - центры. Причиной этого могут быть прежде всего структурные отличия исследованных алмазов. В частности, включения металла-растворителя в зависимости от их количества, размеров и распределения могут заметно видоизменять процессы диффузии примесных атомов, являясь эффективными стоками избыточных вакансий. Это влияние может усугубляться тем, что в ходе термической обработки, как показали визуальные наблюдения, идут процессы миграции и агрегации включений металла в кристалле. [2]
 |
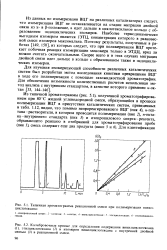
Зависимость константы скорости реакции превращения КНК от кислотности ( сплошные линии - расчетные данные, кружки - опытные данные. [3] |
Исследования кинетики превращения КНК в адипиновую кислоту показывают, что при выборе оптимальной концентрации азотной кислоты и температуры окисления циклогексанола нужно стремиться к подавлению реакции образования 6 6-динитрогексановой кислоты. [4]
Исследование кинетики превращения бензилфенилсульфида в присутствии А1Вг3 показывает [114], что в растворе бензола или хлорбензола с большой скоростью протекает реакция распада тиоэфира. Порядок реакции по тиоэфиру первый, по А1Вг3 - нулевой при избытке катализатора. [5]
Исследование кинетики превращения С-центров в Л - центры под действием температуры показало, что она хорошо описывается феноменологическим уравнением Авраами, которое широко используется для описания процессов распада твердых пересыщенных растворов. Величина параметра процесса п свидетельствует о сферической форме Л - центров, или о прямоугольной и округлой формах пластин. Обращают на себя внимание более высокое значение энергии активации и низкая скорость процесса превращения С-центров в Л - центры. Причиной этого могут быть прежде всего структурные отличия исследованных алмазов. В частности, включения металла-растворителя в зависимости от их количества, размеров и распределения могут заметно видоизменять процессы диффузии примесных атомов, являясь эффективными стоками избыточных вакансий. Это влияние может усугубляться тем, что в ходе термической обработки, как показали визуальные наблюдения, идут процессы миграции и агрегации включений металла в кристалле. [6]
Исследование кинетики превращения цис - и транс-2 5-н-иро - пилтиофана [35, 47], цис - и транс-2 5-диметилтиофана, 2-этилтио-фана, 2-метил-тиациклогексана и тиациклогептана [35] показало, что скорость превращения моноциклических сульфидов с увеличением молекулярного веса возрастает. Алкилтиофаны распадаются медленнее, чем изомерные им 2 5-диалкилтиофаны. Для последних скорости превращения цис - и транс-изомеров мало различаются между собой. [7]
Значительно реже исследование кинетики превращений в структуре стали при ее нагреве и охлаждении производится непосредственно при высоких температурах или при глубоком охлаждении в специальных вакуумных ка: мерах, помещаемых на предметный столик микроскопа. [8]
В табл. 5 приведены результаты исследования кинетики превращения циклогексана, этана и пиперидина в присутствии воды на никелевых катализаторах. В этой работе было выяснено [17], что обе реакции расщепления во всех случаях протекают по нулевому порядку. [9]
Для изучения изомеризующей способности различных каталитических систем был разработан метод исследования кинетики превращения ВЦГ в ходе его полимеризации с помощью газожидкостной хроматографии. [11]
Влияние растворителя изучалось в работе [7], где приводятся данные по исследованию кинетики превращения глюкозы в водно-спиртовых растворах ( вода - этанол и вода - изопропа-нол) в присутствии различных катализаторов. Так, например, в присутствии катализатора 5 % Ru на А12Оз с добавлением к воде этанола ( до 40 %) скорость гидрогенизации возрастает. Увеличение концентрации этанола выше 40 % практически не сказывается на интенсивности процесса. [12]
Имеется лишь эвтектическая точка ( при 42 8 и 58 5 С соответственно), отвечающая содержанию 66 6 % низкоплавкого изомера. Эти диаграммы плавкости использовались для определения степени превращения одного изомера в другой при исследовании кинетики превращения. [13]
Результаты, приведенные в этом разделе, имеют предварительный характер. Их следует рассматривать как иллюстрацию к высказанной идее и как постановку вопроса о возможности применения кинетических хемилюминесцентных методов для определения времени жизни и исследования кинетики превращения активных продуктов электродных реакций. [14]
Несмотря на это, качественное или полуколичественное изучение скорости превращений при высоких давлениях необходимо для промышленности. Большой научный интерес в этой области представляет выяснение влияния негидростатического давления на сдвиговые напряжения при равновесии и исследование кинетики превращений твердое тело - твердое тело. Трудность разделения эффектов обычной метастабильности и медленного протекания реакций от эффектов равновесия в конкретных условиях хорошо иллюстрируется приведенными выше противоречивыми взглядами относительно уплотнения стекол. Тот факт, что и высокое давление, и высокая температура по отдельности и вместе увеличивают скорость реакции, запутывает картину. В течение следующих пяти лет могут быть собраны экспериментальные данные, чтобы однозначно решить этот круг проблем. [15]
Страницы: 1