Исследование - кинетика - растворение
Cтраница 1
Исследования кинетики растворения и процессов кристаллизации в суспензиях двух - и трехкаль-циевого силикатов. [1]
Исследование кинетики растворения титана в соляной кислоте, проведенное в работе Осука [50], показало, что оно протекает с торможением во времени ( фиг. [2]
Для исследования кинетики растворения широко применяют также методы, основанные на растворении компактных образцов определенной геометрической формы, рабочая поверхность которых может быть измерена. [3]
Для исследования кинетики растворения РЬС12 и PbSO4 нами были взяты 6 г РЬС12 при 20 С, 4г РЬС12 при 25 С и 4 36 г PbSO4 при 25 С в 200 мл воды или 200 мл соответствующих растворов. Растворение производилось в специально сконструированном термостате, обеспечившем постоянство температуры с колебаниями 0 5 С. [4]
Для исследования кинетики растворения металлов при нормальном давлении сначала была применена од-носекционная установка, состоящая из реакционного сосуда емкостью 2 л, водяного термостата с нихромовьш нагревателем и терморегулятором и электродвигателя с редуктором, приводящего в движение вал с насаженным на его конец диском. [5]
При исследовании кинетики растворения активированного кварца в бидистиллированной воде в первый час опыта отмечается возрастание рН и электропроводности х и достижение их максимальных значений. В случае неактивированного кварца отмечается незначительное увеличение х и рН ( х38 - 10 - 6 Ом - - см -, рН 7 60) в ходе процесса вследствие выщелачивания стенок стеклянного сосуда. Кривые, характеризующие изменение растворимости активированного кварца во времени, описываются кинетическим уравнением первого порядка. [6]
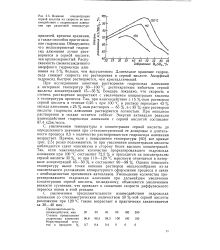 |
Влияние концентрации серной кислоты на скорость ее взаимодействия с гидроксидом алюминия при различной температуре. [7] |
При исследовании кинетики растворения гидроксида алюминия в интервале температур 60 - 100 С десятикратным избытком серной кислоты концентрацией 15 - 35 % Бондарь показано, что скорость и степень растворения возрастают с увеличением концентрации кислоты и температуры процесса. Так, при взаимодействии с 15 % - ным раствором серной кислоты в течение 0 25 ч при 100 С в раствор переходит 43 % оксида алюминия, с 25 % - ным раствором - 85 %, а с 35 % - ным раствором кислоты гидроксид алюминия растворяется полностью. При неполном растворении в осадке остается гиббсит. Энергия активации реакции взаимодействия гидроксида алюминия с серной кислотой составляет 87 4 кДж / моль. [8]
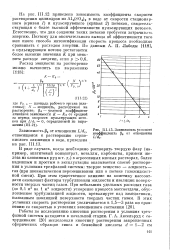 |
Зависимость углового коэффициента 50 от отношения. [9] |
Работы по исследованию кинетики растворения в условиях трехфазной системы находятся в начальной стадии. [10]
Для сравнения были проведены исследования кинетики растворения Ge02 в чистой воде. В соответствии с [2], процесс растворения GeO2 в воде при перемешивании длится около 6 - 7 часов, растворимость оказалась равной 0 494 г на 100 г воды. Возможно, это объясняется какими-то особенностями изучаемой нами двуокиси, так как многократная проверка подтверждала тот же результат. [11]
Вышесказанное давало основание предполагать, что исследование кинетики растворения ковеллина будет затруднено вследствие образования пленки элементарной серы на поверхности диска, менее проницаемой, чем пленка CuS, получающейся при растворении CU2S в цианистых растворах в присутствии кислорода. [12]
Влияние щелочности раствора изучали потому, что при исследовании кинетики растворения серебра и золота было отмечено снижение скорости растворения при повышении щелочности растворов. Условия проведения опытов: температура 25 С, п 150 об / мин, продувка раствора воздухом, концентрация цианида 2 - 10 - 2 моль / л, концентрация щелочи - переменная. [13]
Из анализа характеристических величин, приведенных в табл. 14, а также результатов исследования кинетики растворения и химического анализа продуктов растворения стекол системы мышьяк-сера [82-83] можно сделать следующие заключения. Оптически непрозрачное стекло состава AsSi25 является микронеоднородным. [14]
Метод вращающегося диска обеспечивает хорошую воспроизводимость результатов, что не всегда достижимо при использовании других методов исследования кинетики растворения. [15]
Страницы: 1 2