Исследование - комплексообразование
Cтраница 1
Исследование комплексообразования методом распределения проводится следующим образом. Водный раствор, содержащий ионы металла ( М), в присутствии комплексообразую-щего вещества ( А) экстрагируется органическим растворителем, не смешивающимся с водой. [1]
Исследования комплексообразования в неводных растворах представляют особый интерес для химии комплексов. [2]
Исследование комплексообразования при помощи ионного обмена наиболее удобно проводить с микроконцентрациями элемента, так как зависимость константы обмена от загрузки смолы при малых загрузках несущественна. Кроме того, коэффициенты активности исследуемых ионов в растворе и смоле при поддержании постоянства ионной силы в растворе остаются постоянными. [3]
Исследование комплексообразования между РЗЭ и комплексонами, содержащими различные гетероатомы, показало, что комплексообразующая способность редкоземельных элементов увеличивается в ряду S, N, О, что можно видеть из таблицы. [4]
Исследование комплексообразования в растворе в настоящее время представляет собой одну из основных проблем неорганической химии, о чем свидетельствует огромное количество работ, публикуемых в этой области. Весьма значительное внимание уделяют этому вопросу советские химики. Примером могут служить две монографии - А. [5]
Исследование комплексообразования в системе ванадий ( V) - пирокатехин - пиридин. [6]
Исследование комплексообразования при электрохимических превращениях веществ зависит от того, какая форма ( деполяризатор или продукт) участвует в комп-лексообразовании, и от того, является процесс комплексообразования равновесным или кинетическим. [7]
Исследование комплексообразования иона Fe3 с диоксимом методом распределения было проведено с двл / мя опганическими растворителями: н-амиловым спиртом и хлороформом. Оказалось, что отношение логарифмов коэффициентов распределения не остается постоянным при изменении равновесной концентрации свободного лиганда. Из этого следует, что состав комплексов в водных фазах обеих систем неодинаков. Следовательно, различие в составе этих комплексов может быть обусловлено только наличием в одном из них молекул органического растворителя. [8]
Исследование комплексообразования NpIV в растворах уксусной кислоты проводят путем определения коэффициентов распределения изотопа на катионите при соответствующих условиях. [9]
Исследование комплексообразования Pu ( IIl) в 1 - 5 М НС104 показало отсутствие каких-либо заметных изменений в спектре поглощения. [10]
Исследование комплексообразования спиртов и фенолов. [11]
Исследование комплексообразования диамагнитных центральных ионов возможно и без использования парамагнитных лиган-дов. Ривкинд [5] указывает, что в этом случае можно для определения устойчивости и nL применить своеобразный индикаторный метод. Для этого необходимо пронаблюдать за процессом раз-экранирования какого-либо парамагнитного комплекса в присут - ствии диамагнитного катиона, который образует с данным ли-гандом комплексы более прочные, чем магнитный. Указанный метод использовали Вдовенко и Романов [134] при проверке констант устойчивости фторидных комплексов урана. [12]
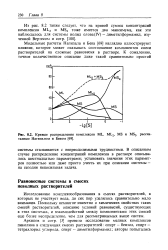 |
Кривые распределения комплексов ML, ML2, MS и MS2, рассчитанные Нагипалом и Беком. [13] |
Исследованию комплексообразования в смесях растворителей, в которых не участвует вода, до сих пор уделялось сравнительно мало внимания. Поскольку немногое - известно о химических свойствах таких смесей растворителей, описание условий равновесий, существующих в этих системах, и взаимодействии между компонентами этих смесей еще более неопределенно, чем для рассматриваемых выше систем. [14]
Для исследования комплексообразования нет необходимости выбирать исключительно чувствительные реакции - важно лишь, чтобы их скорость определялась равновесной концентрацией-ре-агента и чтобы ее можно было легко и достаточно точно измерить. [15]
Страницы: 1 2 3 4