Структурное исследование - кристалл
Cтраница 1
 |
Свойства изоэлектронных веществ.| Свойства этанола и диметилэфира. [1] |
Структурные исследования кристаллов, содержащих водородные связи, показывают, что при связывании атомом водорода двух электроотрицательных атомов А и В ( О, N, F, C1) расстояние между ними ГАВ меньше суммы ван-дер-ваальсовых радиусов. Суммы этих радиусов равны: 00 - 0 28, ON - 0 30, NN - 0 33 нм. [2]
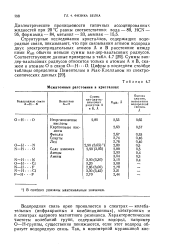 |
Межатомные расстояния в кристаллах. [3] |
Структурные исследования кристаллов, содержащих водородные связи, показывают, что при связывании атомом водорода двух электроотрицательных атомов А и В расстояние между ними RAB обычно меньше суммы ван-дер-ваальсовых радиусов. Суммы ван-дер-ваальсовых радиусов относятся только к атомам А и В, скажем к атомам О в связи О - Н - - О. [4]
Структурное исследование кристалла естественно разделяется а два этапа. [5]
Структурное исследование кристаллов Mo [ Se2C2 ( CF3) a ] 3 было выполнено значительно позднее. Поэтому электронное строение его не было рассмотрено в цитируемых выше работах. [6]
Структурным исследованием кристаллов лизоцима с ингибитором и без него было показано, что ингибитор располагается именно в активных центрах молекулы. Исследование строения кристаллических белков требует большой изобретательности, высокой экспериментальной техники и очень длительного времени. Так, например, исследование строения кристаллов белка рибонуклеазы длится уже 15 лет, а исследование кристаллов инсулина ведется еще дольше - более 20 лет. [7]
В кристаллических структурах отклонения атомов или молекул от положения равновесия происходят только благодаря тепловому движению и малы по сравнению с расстояниями между узлами решетки. Поэтому задачей структурного исследования кристаллов является определение положений узлов решетки. При отсутствии кристаллической решетки отклонения от средних положений велики и поэтому зависимость интерференционной картины от длины волны сказывается особенно резко. [8]
Кроме того, сама глобула представляет собой малоупорядоченное образование из звеньев хаотически свернутой цепной молекулы. Поэтому все обычные методы структурного исследования кристаллов, предназначенные для определения порядка или беспорядка среди малых молекул, будут отчетливо указывать на неупорядоченность системы. Однако такие кристаллы не только имеют вид кристаллов, но и обладают соответствующими термодинамическими свойствами. На этом примере ясно видно расхождение обычных структурных и термодинамических критериев фазового состояния, очень характерное для полимеров, но не всегда учитываемое. Структурные критерии позволяют судить о порядке или беспорядке малых структурных элементов, которые в случае малых молекул просто и являются ими. Термодинамические же критерии чувствительны как к изменению порядка в системах малых структурных элементов, так и в системах больших структурных элементов. Поэтому они совпадают со структурными критериями, когда процесс связан с переупаковкой малых элементов, но расходятся с ними, когда происходит перегруппировка больших структурных элементов без изменения расположения малых элементов. [9]
II, § 3), полное структурное исследование кристалла можно разбить на два принципиально разных этапа. На первом из них решаются проблемы метрики решетки и симметрии кристалла: определяются размеры элементарной ячейки ( а следовательно, и число формульных единиц, приходящихся на ячейку), точечная и пространственная группа кристалла. [10]
Первоначально предполагалось, что описываемые соединения являются геометрическими изомерами. Авторы синтеза считали, что в кристаллах синей формы атомы С1 находятся в / npawc - позиции один к другому, в кристаллах зеленой - в мс-позиции. Однако структурные исследования кристаллов MoOCl2 ( PMe2Ph) 3 синей ( более устойчивой) модификации показали, что именно здесь осуществляется второй вариант расположения атомов хлора. [11]
Страницы: 1