Длина - свободный путь - молекула
Cтраница 3
В процессе сорбции индивидуальных веществ на сорбентах с широким распределением объема пор по радиусам по мере увеличения давления и уменьшения длины свободного пути молекул во все большей части пор молекулярный поток будет переходить в вязкостный. [31]
Кинетическая теория газов позволяет сделать еще чрезвычайно много интересных выводов: о распределении различных скоростей между молекулами газа, о длине свободного пути молекул газа между двумя последовательными столкновениями, о трении газов, о теплопроводности и о теплоемкости их и вообще о законах статистики нестройных молекулярных движений. [32]
Согласно молекулярно-кинетической теории газов теплопроводность не зависит от давления, под которым находится газ, так как плотность газов прямо пропорциональна давлению, а длина свободного пути молекул обратно пропорциональна давлению. Практически теплопроводность реальных газов несколько возрастает с увеличением давления. [33]
По отношению к отверстию, через которое должен проходить газ из объема с большим давлением р в объем с меньшим давлением pz, вакуум считается низким, когда длина свободного пути молекул газа в объеме с большим давлением значительно меньше диаметра отверстия. В этом случае благодаря взаимным столкновениям молекул и проявляющимся в связи с этим силам внутреннего трения и инерции газа наличие отверстия сказывается в газовой среде на относительно большом от него расстоянии. [34]
Это превышение было вначале отнесено на счет поверхностной диффузии, однако, как было показано в более поздней работе Викке и Фоллмера [17], это явление связано с зависимостью скорости потока от длины свободного пути молекул в переходной области течения газа. Викке и Фоллмер, применяя модифицированный метод, исследовали скорость течения водорода, азота, метана и аргона в переходной области через фильтр из иенского стекла и некоторые другие пористые материалы при разных температурах. [35]
Применение манометров, основанных на теплопроводности, возможно потому, что теплопроводность газов остается неизменной при изменении давления газа только до известного предела, именно до тех пор, пока давление не достигнет такой величины, что длина свободного пути молекул газа становится соизмеримой с размерами сосуда. Возьмем сосуд, в котором помещена нагреваемая электрическим током металлическая нить. Если давление газа, окружающего нить, достаточно низко, то уменьшение его влечет за собой уменьшение количества тепла, отдаваемого нитью, что, в свою очередь, вызывает увеличение температуры нити, если приток тепла к ней остается не -, изменным. Увеличение температуры имеет место до тех пор, пока потеря тепла путем теплопроводности газа не увеличится из-за повышения температуры нити настолько, что вновь наступит равновесие между количеством получаемого и отдаваемого тепла. [36]
В выражения для коэффициента диффузии D, внутреннего трения т и теплопроводности х входит значение средней длины свободного пути молекулы А; таким образом, по численным значениям любого из этих трех коэффициентов можно определить среднее значение длины свободного пути молекул А, а отсюда - и эффективный диаметр молекул о. Однако если вычислить для какого-либо газа эффективные диаметры его молекул а по численным значениям всех трех коэффициентов D, г, и х, то получатся несколько различные значения. Эти различия объясняются приближенным характером приведенных теорий. [37]
Но так как объемы IV7, используемые для составления среднего значения интересующих нас величин, все же заключают в себе столь мнэго молекул, чю эти объемы для небольших промежутков времени можно считать за физические индивидуумы, то и вязкие жидкости можно рассматривать как континуумы до тех пор, пока можно полностью пренебречь длиной свободного пути молекул по сравнению с размерами подлежащей исследованию области жидкости. Конечно, чтобы учесть молекулярное движение, необхозимо знать функциональную зависимость молекулярного обмена материи, импульса или энергии от места и времени. [38]
Но так как объемы ДУ, используемые для составления среднего значения интересующих нас величии, все же заключают в себе столь мнзго молекул, чю эти объемы для небольших промежутков времени можно считать за физические индивидуумы, то и вязкие жидкости можно рассматривать как континуумы до тех пор, пока можно полностью пренебречь длиной свободного пути молекул пэ сравнению с размерами подлежащей исследованию области жидкости. Конечно, чтобы учесть молекулярное движение, неотхочимо знать функциональную зависимость молекул р но го обмена материи, импульса или энергии от места и времени. Например, если на дне сосуда, напо. [39]
 |
Передача тепла через газ в условиях низкого вакуума. [40] |
Молекулы газа, ударившиеся в более нагретую пластину, отлетают от нее с большей кинетической энергией, чем до удара. При-достаточно высоких давлениях, когда длина свободного пути молекул X значительно меньше расстояния между пластинами / ( Х СО молекулы уже la расстоянии X от более нагретой пластины встретятся с другими молекулами, которым и отдадут часть своей энергии. Поэтому упрощенно, но принципиально верно можно представить, что газ между пластинами как бы разделен на слои шириной X, в которых вследствие взаимных столкновений и происходит обмен энергиями между молекулами газа. [41]
В условиях высокого вакуума, когда длина свободного пути молекул газа значительно больше диаметра отверстия, осуществляется молекулярный режим перемещения газа, практически без столкновений между молекулами. [42]
Совпадение резулыатов опытов, выполненных в трубах различных диаметров, с теоретически полученным выводом, выражаемым уравнением ( 3), можно рассматривать как экспериментальное подтверждение предположения, что напряжение сдвига пропорционально скорости деформации и что жидкость не скользит вдоль стенок трубы с конечною скоростью, а прилипает к ним. Однако, в сильно разреженных, газах, где длина свободного пути молекул уже не может рассматриваться малою по сравнению с радиусом трубы, наблюдаются отклонения от соотношения ( 3), которые, в соответствии с теорией, могут рассматриваться как результат скольжения молекул вдоль стенок трубы. [43]
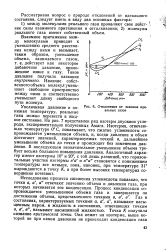 |
Отклонения от законов идеальных газов. [44] |
Наличие собственного объема молекул уменьшает свободное пространство между ними и соответственно уменьшает длину свободного пути молекул. [45]
Страницы: 1 2 3 4