Технический карбид
Cтраница 3
Примеси, особенно свободный углерод и графит, снижают абразивные свойства технического карбида бора, поэтому получаемый в печи продукт подвергают химическому обогащению. [31]
Цнрконовый концентрат в смеси с углем плавят в дуговой печи; при этом образуется технический карбид циркония, а кремний в значительной степени улетучивается в виде SiO2 - В присутствии атмосферного азота или азота, специально введенного в виде газа, образуется смесь карбида и нитрида ( карбонитрид) циркония золотисто-желтого цвета. [32]
Реакция ускоряется в присутствии катализаторов, которыми могут быть некоторые примеси, содержащиеся в техническом карбиде. Чистый СаС2 не реагирует с азотом вплоть до 1200 С. Примеси CaF2, смеси солей NaCl-NaF - Na2SiFe снижают температуру начала взаимодействия до 700 - 800 С. [33]
Этим был однозначно доказан субокисный механизм переноса бора к насыщаемой поверхности при борировании в техническом карбиде бора, и на основании полученных данных разработана простая и экономичная технология борирования сталей в порошке карбида бора в контейнерах с плавким затвором. Эта технология может быть с успехом использована и для борирования тугоплавких металлов и сплавов, обеспечивая намного большие скорости борирования, чем, например, в вакууме, и близкие к скоростям электролизного борирования. [34]
 |
Ацетиленовые генераторы. [35] |
Реакция получения ацетилена из карбида кальция экзотермическая ( выделяется около 400 ккал на 1 кг технического карбида), поэтому необходимо энергичное охлаждение зоны реакции во избежание сильного перегрева, полимеризации и взрыва ацетилена. [36]
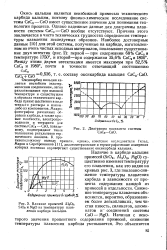 |
Диаграмма плавкости системы СаС2 - СаО.| Влияние примесей АЬОз, SiOa и MgO на температуру плавления карбида кальция. [37] |
Оксикарбид кальция является нестойким экзотермическим соединением легко разлагающимся при высокой температуре и существущим в образцах технического карбида преимущественное виде твердого раствора в каком-либо из компонентов. Микрофотографии различных образцов карбида а также кривые плотности, электропроводности и твердости для системы СаСа - СаО, повиди-мому, подтверждают такое толкование результатов термического анализа. К противоположному выводу пришли, однако, советские исследователи Гельд, Марон и Серебренников [11], дилатометрические и термографические измерения которых косвенно опровергают существование оксикарбида кальция. [38]
Ацетилен-безцветное, газообразное вещество, имеющее неприятный запах светильного газа, когда он выделен из технического карбида; по Муассону, чистый карбид имеет приятный запах. Химически чистый ацетилен содержит 92 3 % углерода и 7 7 / о водорода. Он растворим в воде, в спирте, бензоле и других органических жидкостях. Особенно хорошо он растворяется в ацетоне: при 15 С и под атмосферным давлением 1 об ем ацетона растворяет 25 об емов ацетилена, при - 80 С-около 2000 об емов. Растворимость ацетилена в ацетоне увеличивается с увеличением давления; так, под давлением 12 атмосфер, один литр ацетона растворяет 300 литров его при обыкновенной комнатной температуре. [39]
Одна из основных особенностей производства ацетилена через карбид заключается в том, что несмотря на сложный и непостоянный состав технического карбида, получаемый газ на 99 - 99 8 % состоит из ацетилена ( в пересчете на сухой газ), а основной примесью является просто воздух. Под очисткой ацетилена следует понимать удаление определенных гидридов неметаллов ( как будет подробно показано ниже), и этот процесс не связан с удалением основных примесей, которые часто называют инертными газами, или иногда нерастворимыми ( этот термин менее точен так как их растворимостью в ацетоне или в растворах ацетилена в ацетоне нельзя пренебрегать, стр. [40]
Чистый СаС2 обладает, как показал Франк ( Franck, 1937), решеткой иной структуры, чем загрязненный примесями технический карбид. Последний кристаллизуется, образуя тетрагональную гран сцентрированную решетку, так же как чистый SrC2 и ВаС2 ( см. рис. 88, стр. Карбид кальция, содержащий CaCN2, образует иную решетку. [41]
Чистый СаС2 обладает, как показал Франк ( Franck, 1937), решеткой иной структуры, чем загрязненный примесями технический карбид. Последний кристаллизуется, образуя тетрагональную гранецентрированную решетку, так же как чистый SrC2 и ВаС2 ( см. рис. 88, стр. Карбид кальция, содержащий CaCN2, образует иную решетку. [42]
Чистый СаС2 обладает, как показал Франк ( Franck, 1927), решеткой иной структуры, чем загрязненный примесями технический карбид. Последний кристаллизуется, образуя тетрагональную гравецентрированную решетку, так же как чистый SrC2 и ВаС2 ( см. рис. 88, стр. Карбид кальция, содержащий CaCN2, образует иную решетку. [43]
Тепловой эффект реакции разложения технического карбида жальция слагается из тепла, выделяемого при взаимодействии с водой карбида кальция и содержащейся в техническом карбиде негашеной извести. [44]
Тепло, выделяющееся при разложении технического карбида кальция, представляет собой сумму количеств тепла, выделяемого при взаимодействии с водой карбида кальция и содержащейся в техническом карбиде негашеной извести. [45]
Страницы: 1 2 3 4