Карбонат - тяжелый металл
Cтраница 1
Карбонаты тяжелых металлов Ag, Hg, Pb, Bi, Cu и Fe трудно разлагаются холодной разбавленной кислотой; горячие кислоты легко разлагают их. [1]
К карбонатам тяжелых металлов, способным связывать сероводород, относится и сидерит. [2]
Разложение гидроокисей и карбонатов тяжелых металлов с выделением соответственно воды или углекислого газа имеет место при более высоких температурах и приводит к образованию окислов металлов в состоянии высокой дисперсности. [3]
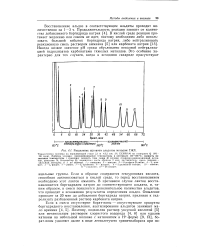 |
Разделение ацетатов альдитов методом ГЖХ. [4] |
Иногда низкое значение рН среды обусловлено неполной нейтрализацией гидролизатов карбонатами тяжелых металлов. [5]
По другому методу отверждающиеся на холоду эмалевые лаки получают, диспергируя резол или резит в растворе жидкого стекла в присутствии МНз или аммиачных комплексов карбонатов тяжелых металлов или гидроокисей тяжелых металлов. На цементе, извести или камне эта смесь превращается в неплавкое покрытие под влиянием света и атмосферных воздействий. Возможно, что значительную роль играет при этом взаимодействие жидкого стекла и материала, на который нанесен лак. [6]
После остывания тигель с плавом помещают в стакан с водой и кипятят до измельчения плава. Двуокись титана и карбонаты тяжелых металлов остаются в осадке, а сульфат натрия переходит в раствор. Карбонаты тяжелых металлов переходят в раствор в виде хлоридов, а двуокись титана остается в осадке на фильтре. Осадок двуокиси титана смывают с фильтра в стакан и растворяют в серной кислоте плотн. [7]
Влияет ли порядок сливания и температура растворов при получении труднорастворимых и легко гидроли-зующихся солей на их состав. Почему при осаждении карбонатов тяжелых металлов чаще используются растворы гидрокарбонатов, а не карбонатов натрия или калия. Существует ли при этом опасность образования кислых солей и загрязнения ими осадков. [8]
Щелочные реагенты удобны тем, что их легче транспортировать и дозировать. В случае применения соды образуется легко отдающий влагу осадок карбонатов тяжелых металлов. Однако сода и щелочь как реагенты дефицитны и дороги, поэтому применяют их, как правило, только в небольших количествах или в виде отходов. Значительно дешевле аммиак, особенно как отход коксохимического производства, притом аммиачные соли легко утилизировать в качестве удобрения. [9]
Севергин указывает также на случаи образования соединений, которые в настоящее время называются комплексными. Так он пишет, что растворы солей меди дают с едкой летучей щелочной солью, то есть с аммиаком, синюю окраску, что осадки карбонатов тяжелых металлов иногда растворяются в избытке карбоната щелочного металла. Ему было также известно, что сульфид мышьяка растворяется в сульфиде натрия, хотя, естественно, никакого представления о сульфосолях в те времена не было. [10]
В практике гальванопроизводства отработанные щелочные растворы часто сбрасываются, так как они являются дешевыми отходами. Однако, такие сбросы нарушают работу очистных сооружений: содержащиеся в обезжиривающих растворах эмульгированные, неэмульгированные и омыленные жиры и масла отравляют ионообменные смолы и мембраны, пассивируют электроды при электрохимических способах очистки, а также нарушают кислотно-щелочной баланс стоков, что при использовании реагентных методов очистки приводит к растворению гидроксидов и карбонатов тяжелых металлов и сбросу их в канализацию. [11]
После остывания тигель с плавом помещают в стакан с водой и кипятят до измельчения плава. Двуокись титана и карбонаты тяжелых металлов остаются в осадке, а сульфат натрия переходит в раствор. Карбонаты тяжелых металлов переходят в раствор в виде хлоридов, а двуокись титана остается в осадке на фильтре. Осадок двуокиси титана смывают с фильтра в стакан и растворяют в серной кислоте плотн. [12]
Состав шлама непостоянен и зависит от применяемых в гальваническом цехе растворов и используемых на очистных сооружениях химикатов. Диапазон содержания всех элементов достигает нескольких порядков. До середины 80 - х годов текущего столетия выделенные из сточных вод осадки гидроксидов и карбонатов тяжелых металлов сбрасывались промышленными предприятиями на городские свалки. Однако с течением времени выяснилось, что дождевыми и талыми водами ( в которых в последние десятилетия повсеместно отмечается снижение величины рН до 4 - 5) со свалок в поверхностные и подземные водные объекты быстро и с достаточной полнотой выносятся ионы тяжелых металлов вследствие легкого растворения гидроксидов в кислых средах. Таким образом, большие трудовые, материальные и энергетические затраты многочисленных предприятий на очистку сточных вод гальванических цехов от ионов тяжелых металлов с экологической точки зрения оказались фактически напрасными. [13]
Страницы: 1