Карбонат - щелочноземельный металл
Cтраница 3
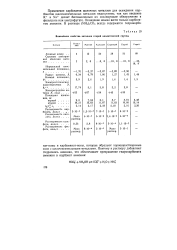 |
Важнейшие свойства катионов второй аналитической группы. [31] |
Применение карбонатов щелочных металлов для осаждения карбонатов щелочноземельных металлов недопустимо, так как введение К и Na делает бессмысленным их последующее обнаружение в фильтрате или центрифугате. [32]
В платиновой чашке растворяют 3 г соответствующего карбоната щелочноземельного металла в горячей разбавленной уксусной кислоте и добавляют затем 40 % - ную плавиковую кислоту. Растворение именно в уксусной кислоте, а не в соляной, имеет весьма существенное значение для получения чистого фторида. Раствор трижды упаривают и каждый раз вновь добавляют плавиковую кислоту. Затем еще раз добавляют 40 % - ную плавиковую кислоту, а также 3 - 5 г NH4F или NH4F - HF. Раствор конденсируют до появления белых паров МРЦР и охлаждают. Твердый осадок разбивают и переносят в платиновую лодочку, которую помещают в реакционную трубку, нагреваемую в трубчатой печи ( см. разд. Для удаления летучих HF, H2O, NH4F продукт медленно нагревают до 400 С в потоке N2 высокой чистоты. Для получения хорошо образованных кристаллов нагревают еще 2 - 3 сут при 700 С в потоке инертного газа. [33]
Один из методов основан на взаимодействии твердых карбонатов щелочноземельных металлов с NH4C1O4 при размалывании их в шаровой мельнице. [34]
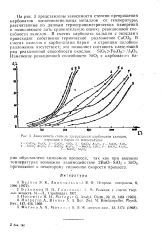 |
Зависимость степени превращения карбонатов кальция, стронция и бария от температуры. [35] |
На рис. 3 представлены зависимости степени превращения карбонатов щелочноземельных металлов от температуры, рассчитанные по данным термогравиметрических измерений и позволяющие дать сравнительную оценку реакционной способности окислов. [36]
Слишком большое количество NH4C1 препятствует полноте осаждения карбонатов щелочноземельных металлов. Это объясняется гидролизом NH4C1, обусловливающим уменьшение рН раствора группового реагента ( МН4) 2СО3до величины, при которой труднорастворимые карбонаты щелочноземельных металлов превращаются в растворимые гидрокарбонаты. [37]
Из таблицы видно, что произведения растворимости карбонатов щелочноземельных металлов приблизительно одинаковы, тогда как произведения растворимости сульфатов и в особенности хроматов резко разнятся. Эти различия в растворимости используются для отделения катионов IV группы друг от друга. [38]
При определении растворимости некоторых солей, например карбонатов щелочноземельных металлов, следует принимать во внимание гидролиз ( см. стр. Так как последний может быть уменьшен прибавлением ОН - ионов, то определение электропроводности должно производиться не в чистой воде, а в разбавленном растворе щелочи. Увеличение электропроводности, вызванное растворением соли, служит тогда для вычисления истинной растворимости. [39]
Опубликованными недавно работами [11-14] было показано, что карбонаты щелочноземельных металлов являются чрезвычайно активными катализаторами полимеризации окиси этилена, позволяющими получить плотный кристаллический высокомолекулярный полимер. Чтобы катализатор был достаточно активным, он должен удовлетворять специфическим требованиям в отношении чистоты, минимального содержания влаги и, возможно, определенной кристаллической формы. Некоторые ионы, например нитрат-ион, должны отсутствовать, поскольку они мешают полимеризации. [40]
Кислоты, в том числе уксусная, разлагают карбонаты щелочноземельных металлов, как и другие карбонаты, с выделением ССЬ. [41]
 |
Растворимость карбонатов щелочноземельных металлов в воде. [42] |
Кислоты, в том числе уксусная, разлагают карбонаты щелочноземельных металлов, как и другие карбонаты, с выделением СОа. [43]
В других работах188 198 200, посвященных исследованию карбонатов щелочноземельных металлов, решающая роль в образовании активных центров полимеризации отводится адсорбции воды. Радиохимическим методом установлено 188 непосредственное участие воды в инициировании полимеризации в результате взаимодействия с высокоэнергетическими центрами поверхности и образования частично ионных состояний. Концентрация таких центров на поверхности SrC03 составляет 1014 на 1 CMZ. Полимеризация окиси этилена на активированном карбонате стронция после резкого автоускорения, связанного с медленным инициированием, протекает стационарно. [44]
В других работах188 - 198 200, посвященных исследованию карбонатов щелочноземельных металлов, решающая роль в образовании активных центров полимеризации отводится адсорбции воды. Радиохимическим методом установлено 188 непосредственное участие воды в инициировании полимеризации в результате взаимодействия с высокоэнергетическими центрами поверхности и образования частично ионных состояний. Полимеризация окиси этилена на активированном карбонате стронция после резкого автоускорения, связанного с медленным инициированием, протекает стационарно. [45]
Страницы: 1 2 3 4