Основной карбонат - цинк
Cтраница 4
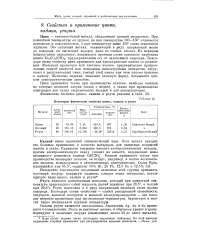 |
Некоторые физические свойства цинка, кадмия и ртути. [46] |
При комнатной температуре он хрупок, но при температуре 100 - 150 отличается ковкостью и пластичностью, а при температуре выше 150 снова становится хрупким. Это активный металл, занимающий в ряду напряжений место до водорода; он вытесняет водород даже из слабых кислот. На влажном воздухе цинк окисляется, покрываясь прочным слоем основного карбоната цинка 7п2С03 ( ОН) 2, предохраняющим его от дальнейшей коррозии. Благодаря этому свойству цинк применяют для предохранения железа от ржавления. Железная проволока или листовое железо, предварительно протравленные серной кислотой или очищенные пескоструйным аппаратом, погружают в расплавленный цинк; тонкий слой цинка при этом плотно пристает к железу. Железные изделия, имеющие сложную форму, покрывают цинком электролитическим способом. [47]
При комнатной температуре он хрупок, но при температуре 100 - 150 С отличается ковкостью и тягучестью, а выше 150 С снова становится хрупким. Это активный металл, занимающий в ряду напряжений место до водорода; он вытесняет водород даже из разбавленных растворов кислот. На влажном воздухе цинк окисляется, покрываясь прочным слоем основного карбоната цинка 2п2СОз ( ОН) 2, предохраняющим его от дальнейшей коррозии. Железную проволоку или листовое железо, предварительно протравленные серной кислотой или очищенные пескоструйным аппаратом, погружают в расплавленный цинк; тонкий слой цинка при этом плотно пристает к железу. Железные изделия, имеющие сложную форму, покрывают цинком электролитическим способом. [48]
Коррозию металлов в воде и водных растворах солей, рН которых находится в интервале 5 - 9, мы условно будем считать процессом, протекающим в нейтральной среде. На практике коррозия металлов происходит очень часто в таких нейтральных средах-в дождевой, речной, грунтовой, морской воде, в растворах солей, используемых в технике. Процесс коррозии большинства металлов в этих средах протекает почти исключительно с участием кислорода в катодной реакции и не сопровождается заметным выделением водорода. Продукты коррозии металлов обычно представляют собой малорастворимые вещества, например гидроокиси железа ( ржавчина), основные карбонаты цинка, свинца и меди, гидроокись алюминия и др. Такие вещества частично экранируют поверхность металла ( например, блокируя катодные участки), в какой-то мере защищая его от дальнейшей коррозии. Однако защитное действие продуктов коррозии черных и многих цветных металлов весьма невелико. Во влажной атмосфере гигроскопичные продукты коррозии не только не защищают металл, но даже способствуют его усиленному разрушению. Поэтому применение ингибиторов коррозии в нейтральных средах является одним из эффективных средств сохранения металла. [49]
При обработке цинксодержащих сточных вод содой цинк осаждается в виде основного карбоната. При этом вначале нейтрализуется серная кислота с образованием угольной кислоты, распадающейся на воду и углекислоту. В дальнейшем сода частично расходуется на нейтрализацию углекислоты до образования бикарбонатов. Если удалить образовавшуюся в результате нейтрализации серной кислоты углекислоту, то обший расход соды со - ответственно уменьшится. При более высоких значениях рН начинается растворение основного карбоната цинка. [50]
Фейткнехт [16] детально изучал продукты коррозии цинка в растворах хлорида натрия. При ближайшем рассмотрении разрушенной поверхности были обнаружены кратеры, заполненные несколькими слоями продуктов различного состава и окруженные концентрическими кольцами основных хлоридов и гидроокисей. Оказалось, что эти основные соли и кристаллические гидроокиси цинка имеют слоистую структуру, в общих чертах аналогичную той, которая приписывается основному карбонату цинка, образующему плотные пленки с хорошей адгезией и имеющему такое важное значение в коррозионной стойкости цинка в атмосфере. Присутствие разных продуктов реакции на прокорродировавшей поверхности говорит о том, что, кроме взаимодействия основных анодных и катодных участков в целом, происходит взаимодействие и между мелкими анодными и катодными элементами. [51]
Этот нейтрализатор разработан фирмой Милчем и получил товарное наименование mil - Gard. Сероводород реагирует с основным карбонатом цинка с образованием нерастворимого в воде сульфида. При температуре 25 С для осаждения 1 моль сульфида натрия требуется 2 6 моль карбоната цинка. При увеличении температуры это соотношение изменяется, и при температуре 65 С 1 моль карбоната цинка связывает уже 1 моль сульфида. Карбонат цинка удаляет сероводород как из кислых растворов, так и из щелочных. Цинк по активности стоит левее железа, поэтому он не является по отношению к нему анодом и не будет увеличивать скорость коррозии стали. В этом отношении основной карбонат цинка явно превосходит основной карбонат меди. Применение основного карбоната цинка наиболее эффективно при удалении небольших количеств сульфидов из буровых растворов с высоким рН, в которых скорость его реакции с сульфидами очень высока. [52]
Страницы: 1 2 3 4