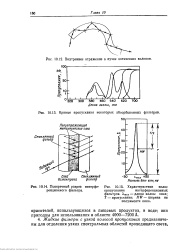
Длина - волна - пик
Cтраница 1
Длина волны пика несколько сдвигается с изменением концентрации. При низких концентрациях максимум пика находится около 12 01 мк. Величина А всегда определяется как расстояние от нулевой линии до точки максимального светопоглощения. [1]
Хтах - длина волны пика; - пропускание; ЯЙ7 - ширина на полу высоте пика. [3]
В табл. 33 длины волн пиков четырех известных полос флуоресценции хлорофиллов а и Ъ в живых клетках сравниваются с длинами волн соответствующих полос в эфирных растворах. [4]
Эти авторы использовали так называемый криофотохими-ческий процесс выращивания металлических кластеров в инертной матрице, с которым стоит ознакомиться поближе. В последнем случае УФ-излучение с длиной волны пика поглощения Agg производит весьма интенсивную эмиссию света точно соответствующую основной полосе эмиссии при возбуждении атомного серебра. [5]
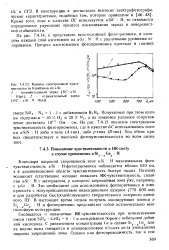 |
Кривые спектральной чувствительности барабанов из a - Si. / - положительный заряд [ Ь С-a - Si.. Н ( р ]. 2 - отрицательный заряд БС - a - Si. N. И ( л 1. [6] |
С увеличением концентрации Се в сплаве SiI JCGejc длина волны пика смещается в длинноволновую область из-за уменьшения ширины запрещенной зоны. [7]
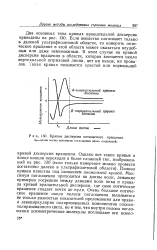 |
Кривые дисперсии оптического вращения. 0-длина волны максимума поглощения обоих соединений. [8] |
Полная кривая известна под названием аномальной кривой. Максимум поглощения приходится на длины волн, лежащие примерно посредине между длинами волн пика и провала кривой вращательной дисперсии, где само оптическое вращение спадает почти до нуля. [9]
Спектрофотометрические кривые фумарина и нарфарина весьма схожи. Однако кривая варфарина имеет пик при 308 мц, а фумарина при 305 ми. В продуктах, которые не мешают определению, например в 5 % концентратах в крахмале, фумармн и варфарин можно различить путем определения длины волны пика поглощения. [10]
Спектрофотометрические кривые фумарина и варфарина весьма схожи. Однако кривая варфарина имеет пик при 308 М ( л, а фумарина при 305 мц. В продуктах, которые не мешают определению, например в 5 % концентратах в крахмале, фумарин и варфарин можно различить путем определения длины волны пика поглощения. [11]
Спектрофотометрические количественные определения обычно проводят в пике спектрального поглощения данного вещества. В статьях приводится общепринятая длина волны для пика спектрального поглощения исследуемого вещества. Известно, что различные спектрофотометры могут давать небольшие отклонения от длины волны этого пика. Практика показывает, что следует использовать длину волны пика, найденную на данном приборе, а не конкретную длину волны, приведенную в статье, при условии, что эти величины отличаются одна от другой не более чем на 0 5 нм в области 240 - 280 нм, , 1 нм в области 280 - 320 нм и 2 нм в области выше 320 нм. Если разница больше, прибор следует повторно калибровать. [12]
На основании химических данных уже давно известно, что op / no - замещенные фенола отличаются от других типов замещенных, а 2 6-замещенные фенола с большими заместителями вообще не участвуют в обычных реакциях фенола и не растворяются в воде. Это объясняется пространственными затруднениями, и можно показать, что у 2 6-ди-замещенных фенола с большими замещающими группами водородная связь не образуется, а у opmo - замещенных фенола с заместителями, размеры которых больше размеров метильной группы, она значительно ослаблена. Сере и Кит-чен [40] опубликовали данные для обширного ряда фенолов различного типа, исследованных в твердом и жидком состояниях и в растворах; они показали, что полоса поглощения ОН появляется, например, у 2 6-ди-тре / п-бутилфенола в положении, которое характерно для несвязанной группы ОН, и что при переходе от раствора к жидкому или твердому состоянию заметного смещения полосы не происходит. Для производных фенола, у которых имеются некоторые пространственные затруднения, наблюдается меньшее изменение длины волны пика ОН по сравнению с несвязанной группой ОН, чем у производных фенола, отличающихся отсутствием пространственных затруднений. Как показал Коггешелл [41], это обусловлено тем, что в первом случае образование связей приводит преимущественно к димери-зации, а не к полимеризации. [13]
В результате предварительного облучения монокристаллов при 77 К УФ - или Х - излучением в видимой области спектра появляется большой пик при 5740 А. Кроме того, в длинноволновой области спектра появляются более слабые пики при 7250 и 7600 А, а в области коротких длин волн ( 3500 А) наблюдается более сильный пик. При постоянной интенсивности излучения пик при 5740 А растет по кинетическому закону первого порядка. Пики, образовавшиеся при 77 К, сравнительно устойчивы при этой температуре, если даже кристаллы облучаются излучением, соответствующим длине волны пика. [14]
Никольс и Хаус с сотрудниками в течение 1915 - 1919 гг. усиленно изучали спектры солей уранила. Они отмечали, что широкие области поглощения ( или группы полос), наблюдаемые для большинства соединений уранила при 20 С, имеют приблизительно постоянные разности частот. Однако Никольс и Хаус отмечали, что интервал между второй и первой полосами коротковолнового конца флуоресцентной системы был равен интервалу, характерному для системы полос поглощения, в то время как интервал между последней и предпоследней полосами длинноволнового конца системы полос поглощения обычно был равен интервалу флуоресцентного ряда. В качестве примера в табл. 1.1 приведены длины волн пиков полос флуоресценции и поглощения K2UO2 ( SO4) 2 - 2H2O при 20 С. Нетрудно заметить приблизительно постоянные частотные интервалы для каждой системы полос, частичное перекрывание трех полос поглощения и флуоресценции, а также наличие в абсорбционной системе интервала Av ( 820 см-1), характерного для флуоресцентного спектра, и во флуоресцентной системе интервала Av ( 661 см-1), характерного для спектра поглощения. Все эти особенности понятны из рис. 1.6. Они указывают на то, что обе системы обязаны своим происхождением одному и тому же электронному переходу ( 20325 см-1), связанному с приобретением колебательного кванта с частотой около 660 см. - 1 в возбужденном и около 820 см-1 в основном состоянии. Это объясняет, почему эти группы полос являются сравнительно слабыми при комнатной температуре и исчезают при низкой температуре, когда в термическом равновесии находятся практически не колеблющиеся молекулы. [15]
Страницы: 1 2