Общая картина - фазовое равновесие
Cтраница 1
 |
Общая картина фазовых равнове - r f. [1] |
Общая картина фазовых равновесий в системах первого типа имеет другой вид. Максимум имеется только на правой части кривых. Область равновесия жидкость - газ не стягивается в точку при критической температуре менее летучего компонента, а переходит в область равновесия газ - газ. [2]
Действительно, разобраться во всей сложности общей картины фазовых равновесий без универсального уравнения состояния можно было только с помощью геометрического метода. [3]
Для разработки и проектирования таких процессов важно знать общую картину фазовых равновесий, включая все их границы ( критич. [4]
 |
Кривая растворимости веществ в сжатых, газах.| Фазовые равновесия в системах жидкость-газ. [5] |
Происхождение минимума и максимума растворимости вещества в газе становится понятным при рассмотрении общей картины фазовых равновесий в двойной системе, построение к-рой стало возможным после обнаружения явления взаимной ограниченной растворимости газов или расслоения газовых смесей. [6]
Как видим, появление дополнительно еще только одной жидкой фазы существенно усложняет общую картину фазового равновесия в двухкомпонентной системе. Очевидно, образование промежуточных твердых фаз в двухкомпонентной системе также должно внести самостоятельный элемент в диаграмму состояния. Как правило, промежуточные твердые фазы формируются на основе определенных химических соединений, которые могут плавиться конгруэнтно либо распадаться в результате перитектического превращения. Обсуждение характера концентрационной зависимости изобарно-изотермического потенциала промежуточных, фаз следует вести в соответствии со строго термодинамически обоснованным понятием фазы. При этом требуется уточнение принадлежности растворов на основе существующих в системе определенных химических соединений к одной или разным фазам. Как известно, природа фаз определяется особенностями межмолекулярного взаимодействия. Последнее в первую очередь обусловлено сортом частиц, их образующих, так как именно природа частиц, образующих данную фазу, обусловливает величину и характер сил обменного взаимодействия, что приводит к формированию вполне определенных химических Связей. Если растворы и фазы различаются родом образующих их частиц ( по сортности), то, следовательно, их химические составы ( речь идет об истинных составах) качественно различны. Следствием этого является тот факт, что термодинамические характеристики фаз, различающихся родом частиц, описываются разными фундаментальными уравнениями. Это очень важное заключение с необходимостью приводит к выводу о том, что такие растворы даже в пределах одной гомогенной системы должны рассматриваться как самостоятельные фазы. Различие между зависимостями свойств растворов, имеющих качественно иные химические составы, от параметров состояния должно проявляться если не в виде функций, то по крайней мере в значениях постоянных величин, фигурирующих в уравнениях этих функций и отражающих специфику межчастичного взаимодействия, а следовательно, и химическую природу сравниваемых растворов. В случае растворов или фаз переменного состава данному качественному составу или, иначе говоря, данному набору частиц по сорту отвечает конечный интервал Количественных составов в данной системе, в пределах которого только и существует строго определенный единственный вид зависимости термодинамических и иных свойств от параметров состояния. Положение о том, что характер зависимости свойств от параметров состояния определяется качественным химическим составом, весьма существенно и названо А. В. Сторонкиным принципом качественного своеобразия определенных химических соединений. [7]
Естественно, что монотектическое и синтектическое трехфазные равновесия вносят самостоятельный элемент в общую картину фазового равновесия двухкомпонентной системы, отличающейся разрывом растворимости в жидком состоянии, поскольку они завершаются стабилизацией либо одного ( рис. 56 а), либо двух ( рис. 56 6) двухфазных равновесий с участием жидких фаз, способных при дальнейшем охлаждении кристаллизоваться и, следовательно, формировать другие трехфазные равновесия - уже эвтектического либо перитектического типа. [9]
Открытие ограниченной растворимости в газовых смесях позволило логически увязать все экспериментальные факты и создать общую картину фазовых равновесий. [10]
Несмотря на то, что приведенные в настоящей работе фазовые диаграммы Р - t, Р - х и Р - t - v в системе ацетилен - нониловый спирт являются качественными, тем не менее они позволяют наглядно представить общую картину фазовых равновесий в системах, которые имеют две области равновесия жидкость - жидкость - газ. [11]
Эксперименты охватывают и двойные [5569-5571, 5583- 5596], и тройные [5597, 5598] системы. В [5583] представлена общая картина фазовых равновесий, в [ 55891 удалось непосредственно наблюдать границу между двумя фазами и измерить на ней поверхностное натяжение. [12]
Эксперименты охватывают и двойные [5569-5571, 5583- 5596], и тройные [5597, 5598] системы. В [5583] представлена общая картина фазовых равновесий, в [5589] удалось непосредственно наблюдать границу между двумя фазами и измерить на ней поверхностное натяжение. [13]
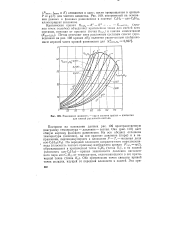 |
Равновесие жидкость - пар в системе пропан - изопентан для смесей различного состава. [14] |
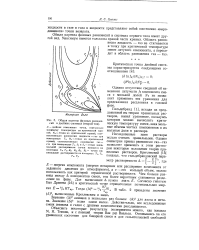
Она ( рис. 110) дает общую картину фазового равновесия. На передней плоскости координатного параллелепипеда ( плоскость чистого пропана) изображена кривая РСЗН, Ф ( 0 обрывающаяся в критической точке С3Н8 ( точка К), а на задней ( плоскость MSO-CsH) - кривая зависимости давления насыщенного пара 30 - C5Hi2 от температуры, оканчивающаяся в его критической точке ( точка Кг) - Обе критические точки связаны кривой точек складки, идущей от передней плоскости к задней. [15]
Страницы: 1 2
