Ди-грег-бутилфенол
Cтраница 1
Ди-грег-бутилфенол ( 19) производят по непрерывной схеме в реакторе колонного типа при 100 С, смешивая изобутилен с фенолом, содержащим катализатор. Алкилирование фенола алкенами-2 протекает труднее, чем алкенами-1, и приводит к смеси ( алкил-2) - и ( алкил-3) производных. [1]
Ди-грег-бутилфенол при 80 - 100 С реагирует примерно в 10 раз быстрее 2 4-изомера. В этом случае основной реакцией является передача трет-бу-тильной группы от 2 6-ди-грет - бутилфенола к фенолу с получением о-трет-бутилфенола, а деалкилирование не идет и в продуктах реакции не накапливается 2 4 6-три-трет - бутилфенол. [2]
 |
Влияние температуры на степень превращения о - ( кривая 1 и rt - грег-бутилфенолов ( кривая 2 в присутствии 0 5 вес. й. й серной кислоты ( продолжительность опытов 60 мин 4Э. [3] |
Присутствие фенола препятствует накоплению ди-грег-бутилфенолов в реакционной смеси до концентрации ( не менее 10 - 16 вес. [4]
Переходя к рассмотрению закономерностей превращений ди-грег-бутилфенолов и их смесей с фенолом в присутствии серной кислоты и сульфокислот, отметим, что наличие двух алкиль ных заместителей повышает по сравнению с моно-грег-алкил-фенолами электронную плотность в ароматическом кольце. [5]
Институтом ВТИ подобрана новая антиокислительная присадка ди-грег-бутилфенол, являющаяся побочным продуктом при производстве н-грег-бутилфенола, для стабилизации трансформаторного масла, очищенного серным ангидридом. [6]
По мнению большинства авторов, наибольшей активностью обладают производные ди-грег-бутилфенолов. [7]
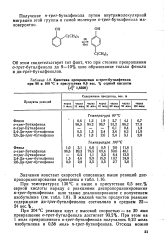 |
Кинетика превращения о-трет-бутилфенола при 80 и 100 С в присутствии 0 5 вес. % серной кислоты. [8] |
Об этом свидетельствует тот факт, что при степени превращения о-грег-бутилфенола до 9 - 10 % шло образование только фенола и ди-грег-бутилфенолов. [9]
Хотя он включает три стадии, выходы на каждой из них высоки, так что суммарные выходы составляют до 65 % даже с ди-грег-бутилфенолами. [10]
Наличие трех грег-бутильных групп объясняет наибольшую реакционную способность 2 4 6-три-грег - бутилфенола в реакциях деалкилирования и диспропорционирования с менее замещенными фенолами по сравнению с 2 6-ди-грег - бутил-п-крезолом и ди-грег-бутилфенолами. [11]
В одинаковых условиях значения суммарного превращения обоих изомеров близки друг другу и линейно увеличивались с повышением температуры от 200 до 300 С. Главной реакцией ди-грег-бутилфенолов было деалкилирование до изобутилена и моно-грег-бутилфенолов. [12]
Бутилфенол в области температур 76 - 220 С ( ниже реакция не шла) вступал в реакцию диспропорционирования ( табл. 1.8 и 1.9) с образованием фенола, 2 4-ди-грег - бутилфе-нола и 2 6-ди-грег - бутилфенола. Кроме того, в результате взаимодействия ди-грег-бутилфенолов с фенолом получался n - грет-бутилфенол, образование которого становилось заметным после того как содержание фенола и ди-грег-бутилфенолов в реакционной смеси достигало 9 - 10 вес. [13]
Моно-грег-бутилфенолы при температуре до 220 С ( область более высоких температур не исследована) сами не деалкили-руются. Эта реакция идет через стадию образования ди-грег-бутилфенолов ( и фенола), в основном 2 4-ди-грег - бутилфенола, и последующего их деалкилирования. Следовательно, как и в случае вгор-бутилфенолов, введение в молекулу моно-грег-бутилфенола второй алкильной группы обусловливает протекание реакции элиминирования грег-бутильной группы. [14]
Бутилфенол в области температур 76 - 220 С ( ниже реакция не шла) вступал в реакцию диспропорционирования ( табл. 1.8 и 1.9) с образованием фенола, 2 4-ди-грег - бутилфе-нола и 2 6-ди-грег - бутилфенола. Кроме того, в результате взаимодействия ди-грег-бутилфенолов с фенолом получался n - грет-бутилфенол, образование которого становилось заметным после того как содержание фенола и ди-грег-бутилфенолов в реакционной смеси достигало 9 - 10 вес. [15]
Страницы: 1